Центры боли в головном мозге
Блокаторы циклооксигеназы работают на периферии. И они вообще не влияют на нервные клетки, поэтому, например, к ним не возникает привыкания и зависимости — по крайней мере, в явном виде. А если вы начинаете использовать вещества, похожие на ГАМК, вещества, похожие на эндорфины, которые будут влиять уже на синаптическую передачу в спинном мозге, здесь вы должны быть готовы к тому, что будет формироваться и привыкание, и зависимость.
Основной группой препаратов из этой категории являются морфиноподобные соединения, потому что морфин — это молекула, которая похожа на эндорфины. С давних времен опиоиды и опиум использовались, для того чтобы снимать боль. К сожалению, морфин и морфиноподобные молекулы вызывают очень быстрое привыкание и зависимость — к сожалению потому, что сейчас мы уже настолько хорошо знаем систему болевой чувствительности, что нам понятно: по-настоящему сильную боль мы можем снимать только морфиноподобными молекулами эффективно и надежно. То есть сама передача сигнала в синапсах, которые в задних рогах серого вещества так организована, что, если мы очень мощно активируем морфиноподобное торможение, мы можем выключить вообще любую боль. Это то, что не способны сделать аспирин, анальгин.
Морфиноподобными препаратами мы можем вообще блокировать болевую чувствительность. При этом не пострадает, например, кожная чувствительность, мышечная, потому что подобный информационный фильтр есть только в тех каналах, которые передают болевые сигналы. Но морфиноподобные молекулы, к сожалению, вызывают очень быстрое привыкание и зависимость. Очень быстро модифицируется работа синапсов, начинает требовать еще, еще и еще эту молекулу. Поэтому, конечно, медицинское использование подобных веществ строго ограничено. Все это сугубо рецептурные препараты, и применять их нужно только в экстренных случаях: при тяжелых ожогах, онкологии или тяжелых физических травмах. Дело усугубляется тем, что морфиноподобные молекулы работают в центрах положительных эмоций, вызывают эйфорию.
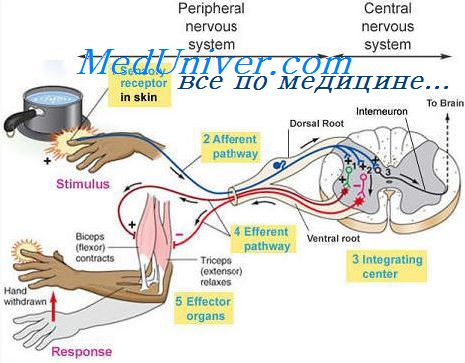
Если болевой сигнал достаточно силен, то он проходит через задние рога серого вещества спинного мозга. Дальше у него две судьбы. Он может запускать реакции, рефлексы на уровне спинного мозга и подниматься в головной мозг. Рефлексы на уровне спинного мозга всем известны — это рефлексы отдергивания. В ситуации, когда вы укололи или обожгли руку и ее отдернули, идет сокращение мышц-сгибателей. Это очень древняя программа, которая носит оборонительный характер, и без этого мы не существуем. Это врожденный рефлекс, мы не обучаемся ему.
А когда сигнал передается в головной мозг, нужны специальные тракты, специальные пути. Аксоны клеток заднего рога серого вещества спинного мозга внутри спинного мозга переходят на противоположную сторону и в боковом канальчике белого вещества поднимаются в головной мозг и достигают таламуса. Таламус — это информационный фильтр на входе в кору больших полушарий, и там есть зрительные центры, слуховые центры, двигательные центры, в том числе центры, связанные с передачей боли. Эти центры находятся во внутренней части таламуса, в медиальных ядрах таламуса. И оттуда сигнал уходит в кору больших полушарий.
Кроме того, часть сигналов идет ниже и достигает гипоталамуса. В гипоталамусе располагаются центры, связанные с нашими потребностями, эмоциями, центры, которые запускают реакцию на стресс. И для этих центров болевые сигналы очень важны. Гипоталамус обеспечивает такое эмоциональное восприятие боли, и наш мозг сконфигурирован таким образом, что боль со стопроцентной вероятностью вызывает негативные эмоции. И чем сильнее боль, тем сильнее эти негативные эмоциональные переживания. Это все логично, это заставляет мозг формировать поведенческие программы, направленные на избегание боли.
За реакцию на боль отвечает в основном задняя часть гипоталамуса, и там находятся нервные клетки, которые запускают изменения в вегетативной нервной системе. Возникает стрессорное состояние, начинает чаще биться сердце, расширяются зрачки, усиливается потоотделение, начинает выделяться адреналин из надпочечников. Кроме того, в задней части гипоталамуса находятся центры, которые активируют оборонительное поведение.
И там еще одна важная развилка. Эта реакция может наступать в виде реакции страха, убегания, избегания, затаивания либо как агрессивная реакция, когда мы как бы нападаем на источник неприятностей. Основной поток болевых сигналов из таламуса поднимается в кору больших полушарий. И здесь есть два варианта.
Первый поток идет специфично в теменную кору, в теменную долю. Это примерно макушка нашей головы, и, если вниз от макушки вот так проводить, вот здесь находятся зоны, которые анализируют чувствительность нашего тела, в том числе здесь есть карта нашего тела, позволяющая оценить болевые сигналы, их интенсивность, специфику, потому что боль бывает разная: острая, тянущая, ноющая.
Кроме того, есть такой тотальный неспецифический поток из таламуса на всю кору больших полушарий, который подтормаживает работу мозга. И специфика болевых сигналов такова, что, когда такой сигнал поднимается в кору, он говорит всем остальным нервным процессам, что нужно прекращаться, нужно разбираться, где болит, где повреждение. В этом смысле боль имеет первый приоритет, и когда у вас что-то заболело, то заниматься какой-то другой деятельностью бывает сложно, особенно если это сильная боль.
Источник
Передача боли в головном мозге. Прерывание болевой импульсации
Полное удаление соматосенсорной коры большого мозга не устраняет способности животного ощущать боль. Следовательно, возможно, что болевые импульсы, поступающие в ретикулярную формацию мозгового ствола, таламус и другие центры нижних отделов головного мозга, вызывают осознанное восприятие боли. Это не означает, что кора большого мозга не играет никакой роли в нормальной оценке боли.
Электрическое раздражение корковых соматосенсорных областей сопровождается ощущением умеренной боли у человека, но это справедливо в отношении лишь примерно 3% стимулируемых точек. Однако даже если болевое ощущение является в основном функцией нижерасположенных центров, полагают, что кора играет особо важную роль в оценке качества боли.
Особая способность болевых сигналов повышать общую возбудимость головного мозга. Электрическая стимуляция областей ретикулярной формации мозгового ствола и внутрипластинчатых ядер таламуса, где оканчиваются пути, проводящие сигналы медленной мучительной боли, оказывает мощное возбуждающее влияние на нервную активность всех областей головного мозга. Фактически эти две области входят в состав основной возбуждающей системы головного мозга. Это объясняет, почему человек практически не может заснуть при наличии у него сильной боли.
Хирургическое прерывание болевых путей. При наличии у человека сильной, не поддающейся лечению боли (иногда в результате быстрораспространяющегося рака), ее необходимо облегчить. С этой целью можно прервать нервные болевые пути в любой из нескольких областей. Если источник боли расположен в нижней части тела, боль часто облегчается на период от нескольких недель до нескольких месяцев с помощью хордо-томии на уровне грудного отдела спинного мозга.
Для этого спинной мозг на стороне, противоположной боли, частично перерезается в его переднебоковом квадранте, что прерывает переднебоковой чувствительный путь. Однако хордотомия не всегда облегчает боль по двум причинам. Во-первых, многие болевые волокна от верхней части тела не переходят на противоположную сторону спинного мозга до тех пор, пока не достигнут головного мозга, а при хордотомии эти волокна не перерезаются.
Во-вторых, через несколько месяцев боль часто возвращается, отчасти в результате сенситизации других путей, которые в норме слишком незначительны и потому неэффективны (например, небольшое число волокон в заднебоковой части спинного мозга). Для облегчения боли экспериментально разработана другая хирургическая процедура, использующая катетеризацию специфических болевых областей во внутрипластинчатых ядрах таламуса, что часто облегчает мучительную боль, в то же время не изменяя восприятие острой боли — важного защитного механизма.
— Также рекомендуем «Обезболивающая система. Подавление болевой импульсации»
Оглавление темы «Боль. Пути и механизмы передачи боли»:
1. Функция таламуса в соматических ощущениях. Корковый контроль чувствительности
2. Боль. Классификация боли — быстрая и медленная боль
3. Поражение ткани и боль. Ишемия как причина боли
4. Пути передачи болевых сигналов. Передача боли в спинном мозге
5. Палеоспинальный путь передачи боли. Палеоспиноталамический путь боли
6. Передача боли в головном мозге. Прерывание болевой импульсации
7. Обезболивающая система. Подавление болевой импульсации
8. Торможение проведения болевых сигналов. Электрическая стимуляция при боли
9. Причины висцеральной боли. Париетальная боль
10. Локализация висцеральной боли. Пути передачи висцеральной боли
Источник
Всё о том, как возникает это чувство и можем ли мы им управлять.
Откуда берётся боль
Боль — это эволюционно выгодный механизм. Она сообщает о повреждениях, которые требуют внимания: «Проблема! Сделай что-нибудь, а то мы истечём кровью».
Чтобы механизм был эффективным, боль должна правильно отображать характер повреждений, но это происходит далеко не всегда. Одно и то же повреждение может ощущаться по-разному, а иногда вообще не чувствоваться. Например, увлёкшись каким-то делом, вы можете не заметить, что порезались. Нервы мгновенно передают сигнал о повреждении, а вы замечаете порез, только когда видите кровь.
В то же время люди могут чувствовать несуществующие повреждения. Например, в своей книге «Мозг рассказывает» профессор нейрофизиологии Вилейанур Рамачандран описывает своего пациента, который чувствовал боль в сжатом кулаке ампутированной руки. Когда с помощью системы зеркал пациент увидел отражение другой руки и разжал кулак, фантомная боль исчезла.
Есть ещё один хороший пример : строителю в ботинок воткнулся длинный гвоздь. Любое движение гвоздя вызывало сильную боль, и, чтобы вытащить его, строителю дали обезболивающее. Когда гвоздь извлекли и сняли ботинок, оказалось, что нога не повреждена. Гвоздь прошёл между пальцев, не задев кожи. Бедняга тут же исцелился.
Этот и многие другие случаи доказывают, что мозгу далеко до объективности. Да, наши ощущения сильно зависят от рецепторов, но не только от них. Рецепторы не могут быть субъективными: они честно отсылают данные о том, что произошло в тканях, а вот как это интерпретирует мозг — совсем другой вопрос.
Мы разберём, какие механизмы ответственны за восприятие боли и ошибки в интерпретации, как она возникает и путешествует по нервным клеткам организма.
Как в мозге рождается боль
Сигналы передаются от рецепторов в спинной мозг
В своей статье о боли нейробиолог Гермес Солензол (Hermes Solenzol) описал, как боль добирается от рецепторов до мозга.
Болевые рецепторы — ноцицепторы — состоят из миллиардов нервных волокон разных типов. Более крупные А-волокна передают быструю боль, например от укола иглой. Мелкие С-волокна чуть запаздывают и передают сигналы о более медленной и продолжительной боли. Вместе эти рецепторы обеспечивают чувствительность кожи, мышц, суставов, глубоких тканей и внутренних органов.
Тела нейронов, отдающих нервные волокна любого типа, лежат в спинномозговых ганглиях — нервных узлах, расположенных по бокам спинного мозга. Через них информация о повреждении попадает в задний корешок спинного мозга. При этом один сигнал может подавлять другой.
Например, длительная тупая боль, доставляемая медленными волокнами типа С, может подавляться быстрым уколом или щипком, который передают быстрые А-волокна. Вы просто перестанете чувствовать тупую боль, хотя её источник никуда не денется.
По этой же причине мы инстинктивно потираем больное место: касание и надавливание передают другие тактильные ощущения, которые снижают чувство боли.
Сигналы обрабатываются в головном мозге
Из спинного мозга сигнал попадает в головной мозг: через ствол мозга в таламус — центральный процессор всей сенсорной информации. В разных ядрах таламуса обрабатываются визуальные данные, звук, тактильные ощущения.
Из таламуса сигнал уходит в три области мозга:
- Соматосенсорную кору. Эта структура устанавливает, из какой части тела пришёл сигнал о боли.
- Островковую долю, или островок. Именно за счёт островка мы понимаем, насколько сильна боль, и испытываем по поводу неё какие-либо эмоции. Кроме того, островок играет роль и в формировании других эмоций: печали, радости, злости, отвращения, эмпатии и даже любви. Возможно, поэтому эмоции сильно влияют на восприятие боли. Доказано, что влюблённость снижает её: когда люди держатся за руки, боль стихает .
- Переднюю поясную кору (ППК). Эта структура мозга связана со знаниями, устранением ошибок и конфликтов, вниманием и мотивацией. За счёт неё появляется стимул что-то сделать с болью (или не делать ничего). ППК решает, какие действия мы будем предпринимать, исходя из текущего положения дел.
Как видите, не существует горячей линии, по которой сигнал о повреждении доходил бы до мозга. Он проходит через столько сложных и многофункциональных структур, что легко может притупиться или, наоборот, развернуться на полную. При обработке сигналов мозг определяет его значимость, исходя из ситуации, предыдущего опыта, влияния культуры, ваших знаний и сенсорной информации: звука, запаха, картинки.
Боль — это не объективное ощущение, а вольная интерпретация мозга. Боль рождается именно в нём.
Можем ли мы управлять болью? Напрямую нет. Не забывайте, что ваше «я» — это тоже продукт мозга, один из его процессов. Поэтому вы управляете своим мозгом не больше, чем движение стрелки часов управляет механизмом этих часов.
Но мы можем что-то сделать, чтобы притупить чувство боли, через управление своими эмоциями и создание подходящей обстановки.
Как облегчить боль
Создайте комфортную обстановку
Мы описали только восходящие пути боли — от периферии в мозг, но существуют и обратные, нисходящие пути. Мозг не только определяет, как вы будете чувствовать боль, но и может влиять на чувствительность нервов: понижать её или повышать.
Когда вы нервничаете, мозг считает, что обстановка опасная. Поэтому он заставляет периферические нервы передавать ему больше информации. В результате вы острее чувствуете боль даже от незначительных стимулов.
Но мозг может сделать и обратное: если вы спокойны и находитесь в безопасности, периферические нервы могут воспринимать меньше стимулов и вы будете чувствовать меньше боли. Это выяснили ещё во время Второй мировой войны: солдаты чувствовали гораздо меньше боли, чем должны были при своих травмах, потому что были счастливы оказаться в безопасности, а не на поле боя.
Поверьте в то, что не будет больно
Воспринимайте события позитивно. Люди с быстрым эмоциональным восстановлением действительно чувствуют меньше боли.
Измените тактильные ощущения
Рецепторы в коже предают не только сигналы о боли, но и другие ощущения: касания, давление, холод, тепло. Поэтому многие практики вроде растирания, согревания или охлаждения, перетягивания бинтами или наклеивания тейпов помогают унять боль, не влияя при этом на её причину.
Попробуйте изменить тактильные ощущения в болезненной области, и боль тоже изменится.
Не драматизируйте
Поскольку боль — личное переживание, некоторые люди, чтобы передать её интенсивность, прибегают к художественным описаниям и чересчур драматизируют: «Боль впивается в меня раскалёнными иглами», «Боль полыхает пожаром».
Такие фразы вызовут сочувствие со стороны других людей, но могут обернуться против самого рассказчика. Описав боль красочными фразами, вы убеждаете свой мозг, что так оно и есть, и начинаете чувствовать свои фантазии.
Боритесь со страхом через знания
Неизвестность вызывает страх и тревожность, а они увеличивают восприятие боли. Если вас мучает боль неизвестного характера, сразу же сходите к врачу и узнайте от него максимум о своём заболевании.
Если он не дал достаточно информации, сходите к другому доктору или поищите научные труды на эту тему. Сделайте всё, чтобы успокоиться и почувствовать, что с вами в целом всё в порядке. Доказано , что знание причины боли помогает её уменьшить.
Не терпите боль: это может плохо закончиться
Дело даже в не том, что вы можете запустить какое-то опасное заболевание. Нервные рецепторы привыкают к боли и становятся более восприимчивыми. Не доводите до структурных изменений в нейронах, сделайте всё, чтобы избавиться от боли, пока она не переросла в хроническую.
Читайте также
- Как стресс влияет на мозг →
- Механизм страха: как отучить мозг бояться →
- Как меняется мозг в течение менструального цикла →
Источник
Представлен различными отделами коры больших полушарий переднего мозга, особенно, первой соматосенсорной зоной (постцентральной извилиной теменной доли), а также второй соматосенсорной зоной (области сильвиевой борозды височной коры и фронтальной корой) и даже сенсорной зоной затылочной коры.
Именно в этих корковых структурах с участием различных центральных механизмов формируется специфическое ощущение боли. Корковые центры боли тесно связаны обратными связями с таламусом, гипоталамусом, ретикулярной формацией, лимбическими, вегетативными, эндокринными и двигательными (экстрапирамидными и, особенно, пирамидными) центрами, а через них со спинным мозгом и далее через эфферентные соматические и вегетативные нервные волокна с исполнительными органами и тканями организма.
Основные реакции организма на боль реализуются в виде отрицательных эмоций, осознанных мотиваций устранения болевых ощущений и осознанного поведения, направленного на более быстрое и эффективное не только избавление организма от повреждающего фактора, но и лечения поврежденных структур организма. Реакции организма на боль реализуются также в виде активизации механизмов памяти, направленных как на избегание болезнетворных факторов в будущем, так и закрепление опыта по лечению ран.
40.10. структурно-функциональная организация
антиноцицептивной системы
Фактически интенсивность и характер специфического болевого ощущения определяется не только активизацией ноцицептивной (НЦС), но и степенью и характером функционирования антиноцицептивной системы (АНЦС).
В процессе эволюции шло совершенствование как НЦС, так и АНЦС. В физиологических условиях обе эти системы функционируют содружественно. Активизация НЦС под влиянием многообразных ноцицептивных раздражителей всегда стимулирует АНЦС, что ограничивает болевую афферентацию, болевое ощущение и многочисленные поведенческие, вегетативные и метаболические реакции организма, а значит способствует более быстрому и эффективному восстановлению нарушенных структур и функций.
АНЦС, как и НЦС являются гетерогенными нервными образованиями (сегментарными в спинном мозге и надсегментарными в головном мозге: различных структурах ствола мозга, особенно в промежуточном мозге и коре больших полушарий) болевой чувствительности. Антиноцицептивные структуры и механизмы располагаются на всех переключательных станциях НЦС.
Функционирование АНЦС определяется опиоидными и неопиоидными механизмами, ответственными за ограничение как болевой афферентации, так и болевого ощущения в ответ на действие самых различных по природе интенсивных алгогенных раздражителей.
Опиоидная система регуляции боли включает опиатные рецепторы и опиоидные пептиды.
Опиатные рецепторы представлены мю-(m), сигма- (s) и каппа (k)-рецепторами. Эти рецепторы имеются во всех структурах НЦС, главным образом, в основных релейных станциях афферентации ноцицептивной импульсации (желатинозной субстанции задних рогов спинного мозга, гигантоклеточном ядре продолговатого мозга, центральном сером околоводопроводном веществе и покрышке среднего мозга, синем пятне, черной субстанции, красном ядре, ядрах ретикулярной формации, гипоталамуса и таламуса, лимбических структур, а также в корковых центрах боли. В одних образованиях ЦНС (фронтальной коре, лимбических структурах) опиатных рецепторов во много раз больше, чем в других (теменной, височной и затылочной долях).
Опиоидные пептиды представлены эндорфинами и энкефалинами.
Эндорфины (a, b, g) выполняют роль медиаторов АНЦС и имеют в ЦНС более узкую локализацию их синтеза и действия. В гипоталамусе, гипофизе, перегородке мозга, среднем мозге, таламусе эндорфинов определяется значительно большее количество, чем энкефалинов.
Энкефалины выполняют роль и медиаторов, и модуляторов. Они имеют более обширную локализацию их синтеза и действия в ЦНС. Причем, энкефалины оказывают общее угнетающее действие на активность различных нейронов ЦНС, снижая их реакции на любой сенсорный раздражитель. В отличие от эндорфинов, энкефалины оказывают более слабое угнетающее действие на ЦНС.
Эндорфины, как и экзогенный морфин, оказывают угнетающее влияние на ноцицептивные синаптические входы, а также активируют большинство нейронов АНЦС. Таким образом, эндорфины снижают болевую чувствительность и болевое ощущение не только за счет угнетения структур НЦС, но и за счет активизации структур АНЦС. Следует подчеркнуть, что эндогенная опиоидная система с участием эндорфинов, энкефалинов и опиатных рецепторов является надежным регулятором и контролером интенсивности ноцицептивного возбуждения. С увеличением интенсивности ноцицептивной импульсации опиоидная система активизируется в большей степени. Не нарушенная опиоидная система всегда находится в активном состоянии и способна ограничивать степень возбуждения различных сенсорных, в том числе и болевых структур.
Отмечено, что содержание опиоидных пептидов в биосредах организма, особенно в структурах АНЦС, как и активность опиатных рецепторов в различных образованиях этой системы подвержены суточным колебаниям. Этим, вероятно, и объясняются отмечаемые суточные ритмы болевой чувствительности.
Показано также, что опиатные рецепторы образуют обратимую связь с наркотическими аналгетиками. Последние могут быть вытеснены их антагонистами, итогом чего является восстановление болевой чувствительности. Налоксон блокирует, главным образом, (m)-опиатные рецепторы, в меньшей степени (в 10 раз) – s- опиатные рецепторы, и в наименьшей степени (в 30 раз) – k-опиатные рецепторы. Наряду с антагонистами опиоидных пептидов найдены также их агонисты.
Механизм обезболивающего действия опиоидных пептидов заключается в том, что после взаимодействия эндорфинов и энкефалинов с опиатными рецепторами не проявляется алгогенное действие субстанции Р и других алгогенов.
Механизм действия налоксона, имеющего меньший, чем опиоидные пептиды размер молекулы, заключается в более быстрой и более сильной связи с опиатными рецепторами, в результате чего опиоиды не могут с ними взаимодействовать, а значит оказывать обезболивающее действие.
Неопиоидная система регуляции боли включает следующие гуморальные механизмы, реализующие свое действие через:
§ нейротензин гипоталамуса, ядер шва ствола мозга, центрального серого окловодопроводного вещества (ЦСОВ) и других стуктур ЦНС. Причем, обезболивающий эффект нейротензина оказался во много (100-1000 раз) более сильным, чем у энкефалинов. Причем этот эффект, в отличие от опиоидных пептидов, не купируется налоксоном;
§ окситоцин, вырабатываемый, главным образом, крупноклеточными ядрами переднего гипоталамуса;
§ ангиотензин-II, образующийся из ангиотензина-I;
§ серотонин и серотониновые рецепторы;
§ норадреналин и центральные α-адренорецепторы;
§ ацетилхолин и центральные М- и Н-холинорецепторы;
§ гамма-аминомасляная кислота (ГАМК) и ГАМК-рецепторы;
§ глицин и глициновые рецепторы.
Серотонинергические механизмы снижения боли представлены преимущественно в ядрах шва ствола мозга, ЦСОВ, медиальном гипоталамусе, таламусе и других структурах ЦНС. Различные медиаторы (норадреналин, дофамин) и ФАВ, активизирующие синтез, выделение и действие серотонина, стимулируют опиатную аналгезию.
Адренергетические механизмы угнетения боли представлены структурами сегментов спинного мозга и ствола головного мозга. Эффект норадреналина реализуется через возбуждение a-адренорецепторов. Это приводит к угнетению болевой импульсации и активизации опиатных механизмов.
Холинергичексие механизмы ослабления боли представлены различными структурами ЦНС, ососбенно среднего мозга и ЦСОВ. Активация центральных Н- и М- холинорецепторов ослабляет боль, усиливает морфиновую анестезию, стимулирует высвобождение опиоидных пептидов.
ГАМК- и глицинергетические механизмы обезболивания представлены многими структурами ЦНС (головного и спинного мозга). Показано, что в ответ на боль последними усиливается выделение и действие медиаторов торможения ГАМК и глицина, которые возбуждая ГАМК и глициновые рецепторы, ослабляют болевое ощущение, а также поведенческие и эмоциональные реакции на болевое воздействие.
Дата добавления: 2015-04-30; просмотров: 790; Опубликованный материал нарушает авторские права? | Защита персональных данных | ЗАКАЗАТЬ РАБОТУ
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Да какие ж вы математики, если запаролиться нормально не можете??? 8599 — | 7443 — или читать все…
Читайте также:
Источник

