Головокружение в практике врача
Головокружение — один из наиболее часто встречающихся в медицинской практике симптомов. Описано около 80 заболеваний, при которых возможно появление головокружения. В амбулаторной практике головокружение является основным поводом обращения к врачам различных специальностей в 2–5% случаев, а применительно к терапевтам эти цифры нужно, как минимум, удвоить.
Вестибулярные нарушения сосудистого, токсического, инфекционного и другого генеза могут быть обусловлены различными соматическими заболеваниями. Наиболее частыми причинами возникновения вестибулярного синдрома являются гипертоническая болезнь, шейный остеохондроз, церебральный атеросклероз. Вестибулярная дисфункция является почти обязательным симптомом при опухолях, воспалительных, дегенеративно-дистрофических, наследственных заболеваниях центральной нервной системы, черепно-мозговой травме, вибрационной болезни.
При обследовании больного с жалобами на головокружение прежде всего нужно выяснить, что он называет головокружением. Это поможет врачу установить характер головокружения, то есть вестибулярное оно или невестибулярное. В зависимости от характера головокружения врач определяет требуемый объем исследований и необходимость привлечения тех или иных консультантов (невропатолога, окулиста, оториноларинголога, гематолога и других).
Вестибулярное головокружение, как правило, бывает системным. Такое головокружение описывается больным как ощущение движения собственного тела вокруг одной из осей трехмерного пространства, либо ощущение движения предметов вокруг одной из осей, либо то и другое одновременно.
Невестибулярное головокружение характеризуется больными как чувство опьянения, надвигающейся потери сознания, легкости в голове, неустойчивости при ходьбе, тошноты, ощущения пелены, потемнения в глазах.
В большинстве случаев периферические вестибулярные расстройства обусловлены доброкачественным пароксизмальным позиционным головокружением, болезнью Меньера, лабиринтитом или инфарктом лабиринта, редко — вестибулярным нейронитом или невриномой VIII нерва, расположенной в пределах внутреннего слухового прохода. Следует иметь в виду, что поражение лабиринта может наблюдаться при сифилисе, ВИЧ-инфекции, нарушении обмена веществ, болезни Педжета, при аутоиммунной, аллергической и наследственной патологии.
Поражение центральных отделов вестибулярного анализатора наблюдается при вертебробазилярной недостаточности, инфарктах варолиева моста, продолговатого мозга или мозжечка, опухолях мостомозжечкового угла и задней черепной ямки, при арахноидите, стволовых энцефалитах, при кистах мозжечка, выраженной внутричерепной гипертензии, при дегенеративных заболеваниях центральной нервной системы, височной эпилепсии.
Важное место в патогенезе вестибулярных нарушений занимают дисциркуляторные расстройства в вертебробазилярной системе (ВБС), которая кровоснабжает как периферический, так и ядерный уровень вестибулярного анализатора.
Факторы, ограничивающие кровоток в ВБС, весьма разнообразны: экстравазальная компрессия суставными отростками при нестабильности шейного отдела позвоночника или остеофитами в унковертебральных областях, рефлекторный спазм артерий при раздражении остеофитами периартериального симпатического сплетения, тромбозы, эмболии, сдавление сосудов мышцами шеи, рудиментарными шейными ребрами (Н.?В.?Верещагин, 2001). У лиц среднего и пожилого возраста наиболее частыми причинами нарушения мозгового кровообращения, в том числе и кровообращения в ВБС, являются атеросклероз и гипертоническая болезнь.
Окклюзирующие атеросклеротические стенозы могут значительно нарушать кровообращение как в магистральных сосудах головного мозга, вызывая симптоматику центральной вестибулярной дисфункции, так и в лабиринтной артерии, воспроизводя клинику периферических кохлеовестибулярных расстройств. Атеросклеротические изменения в сосудах внутреннего уха, а также в сосудах головного мозга, приводящие к дегенерации слуховых путей и ядер, лежат в основе старческой тугоухости.
Развитие хронической цереброваскулярной недостаточности при гипертонической болезни обусловлено морфологическими изменениями в сосудистом русле и нарушениями реологических свойств крови.
Морфогенез сосудистых изменений при артериальной гипертонии хорошо изучен. В первой («доклинической») стадии развивается гипертрофия гладкомышечных клеток и эластических волокон в артериолах и мелких артериях. Во второй стадии, при которой артериальное давление стойко стабилизируется на повышенных показателях, происходит своеобразная структурно-функциональная перестройка сосудистой стенки, которая начинается с плазматического пропитывания ее структур, что в дальнейшем приводит к развитию склероза и гиалиноза в артериолах и мелких артериях многих органов, прежде всего, головного мозга, почек, сетчатки глаза, надпочечников. В более крупных артериях (аорте, артериях мышечно-эластического типа и наиболее крупных стволах мышечного типа) развивается эластофиброз и артериосклеротический процесс. В третьей стадии на первый план выступают связанные с сосудистыми изменениями вторичные поражения органов. Они обусловлены нарушениями внутриорганного кровообращения и могут развиваться как остро (кровоизлияния, инфаркты), так и медленно (атрофия, склероз органов).
Не менее важным фактором развития хронической цереброваскулярной недостаточности при гипертонической болезни являются нарушения реологических свойств крови (склонность к гиперкоагуляции, повышение вязкости цельной крови, предела текучести, гематокритного числа, изменение интенсивности агрегации эритроцитов и их деформируемости).
Вестибулярные расстройства у больных гипертонической болезнью могут носить различный характер. При подъемах артериального давления, усугубляющих ишемию центральных отделов вестибулярного анализатора, у больных возникает чувство потери равновесия, проваливания, падения, неровного пола, уплывания окружающих предметов. В ряде случаев вестибулярные нарушения протекают в виде острого вестибулярного криза, клиническая картина которого зависит от того, в какой области происходят сосудистые расстройства (во внутреннем ухе, задней черепной ямке или в более высоких отделах центральной нервной системы).
Острое нарушение кровообращения (тромбоз, эмболия) в лабиринтной артерии или кровоизлияние в ушной лабиринт проявляется сильнейшим, внезапно возникшим головокружением, тошнотой, рвотой, расстройством равновесия и координации движений. Одновременно появляется шум в одном ухе и резкое снижение слуха, вплоть до полной глухоты. Это состояние называют апоплексией лабиринта. Апоплексию лабиринта следует дифференцировать с приступом болезни Меньера и инсультом. В отличие от болезни Меньера, протекающей с повторными приступами головокружения, при апоплексии лабиринта наблюдается однократный вестибулярный криз, влекущий за собой стойкую глухоту на одно ухо, что не характерно для болезни Меньера. От инсульта апоплексию лабиринта отличает отсутствие очаговых неврологических симптомов.
Острое нарушение кровообращения в вертебрально-базилярном бассейне, приводящее к ишемии в области вестибулярных ядер, также вызывает возникновение тяжелого приступа вестибулярной дисфункции. Приступ вестибулярной дисфункции при ишемии вестибулярных ядер проявляется сильным головокружением с тошнотой, рвотой, расстройством равновесия, как правило, присутствует очаговая неврологическая симптоматика. Слуховые расстройства в этих случаях могут отсутствовать либо проявляются двусторонним снижением слуха и шумом в ушах. Односторонних слуховых расстройств, присущих апоплексии лабиринта, в этих случаях не бывает, поскольку проводящие пути слухового анализатора на уровне слуховых ядер частично перекрещиваются. Отличительной чертой вестибулярного ядерного криза является длительность сохранения вестибулярных нарушений. При периферических вестибулярных синдромах компенсация вестибулярной функции развивается гораздо быстрее благодаря функциональной сохранности вестибулярного ядерного комплекса.
Еще один вариант вестибулярной дисфункции, возникающей на фоне гипертонической болезни,?— формирование ограниченных инсультных очагов в полушариях мозжечка, которые обнаруживаются при МРТ-исследованиях, а клинически проявляются лишь системным головокружением и кратковременной атаксией без общемозговых и стволовых симптомов (С.?А.?Афанасьева и соавт., 2003). Однако чаще недостаточность кровообращения в ВБС на фоне гипертонической болезни проявляется статической и динамической атаксией в виде неустойчивости и пошатывания при ходьбе при незначительных нарушениях координации движений (Н.?В.?Верещагин, 2001).
В профилактике и лечении вестибулярных нарушений при гипертонической болезни и атеросклерозе большое значение имеет стабилизация артериального давления. Однако, как показывает практика, вестибулярная дисфункция у этой группы больных требует дополнительных мер воздействия. Следует отметить, что церебральные вазоактивные препараты зачастую не дают желаемого эффекта вследствие наличия описанных выше грубых изменений в стенках сосудов. В этих условиях препаратами выбора являются лекарственные средства, повышающие адаптационные возможности вестибулярного анализатора к условиям хронической гипоксии.
Известно, что некоторые группы фармакологических препаратов (ноотропы, антигипоксанты, антиоксиданты, стресс-протекторы, психостимуляторы и др.) оказывают регуляторное влияние на механизмы адаптации, ускоряя развитие адаптационно-компенсаторных реакций в центральной нервной системе. Однако для купирования симптомов вестибулярной дисфункции необходимо назначение препаратов, нормализующих передачу нервного импульса непосредственно в структурах вестибулярного анализатора.
С целью идентификации нейромедиаторов, участвующих в процессе восстановления вестибулярного равновесия, проведены экспериментальные иммунохимические исследования (M.?Lacour, B.?Tighilet, 2000). Установлено, что у животных после односторонней перерезки вестибулярной порции VIII нерва наблюдается заметное и устойчивое снижение содержания гистамина в вестибулярных ядрах, что говорит о повышенном высвобождении его. Это снижение было значительно более выражено у животных, получавших антагонисты гистаминовых рецепторов (бетагистин, тиоперамид), одновременно в этой группе отмечалось достоверное ускорение процесса восстановления вестибулярной функции. Полученные данные доказывают, что увеличение высвобождения гистамина способствует развитию вестибулярной компенсации.
Препаратом, целенаправленно влияющим на развитие вестибулярной компенсации, является бетагистин (Бетасерк).
Действие Бетасерка (структурного аналога гистамина) реализуется через гистаминовые рецепторы.
В настоящее время известны три типа гистаминовых рецепторов: Н1, Н2 и Н3. Рецепторы Н1 и Н2 являются постсинаптическими, Н3 — пресинаптическими. Н3-рецепторы расположены в основном в центральной нервной системе. В норме выделение гистамина приводит к стимуляции всех видов гистаминовых рецепторов (Н1, Н2 и Н3). Взаимодействие гистамина с Н3-рецепторами, расположенными в пресинаптической мембране гистаминергического синапса, препятствует дальнейшему выбросу медиатора по принципу обратной связи.
Бетасерк в центральной нервной системе является умеренным агонистом Н1-рецепторов и сильным антагонистом H3. Введение Бетасерка значительно увеличивает выделение гистамина за счет блокирования Н3-рецепторов и способствует развитию процессов компенсации в вестибулярном анализаторе, что проявляется исчезновением симптомов вестибулярной дисфункции (головокружения, нарушения равновесия, вегетативных нарушений и др.).
Бетасерк вызывает не только высвобождение гистамина, но и активизирует его синтез в вестибулярных ядрах, что также способствует развитию восстановительных процессов. В связи с этим следует отметить нецелесообразность одновременного назначения больным Бетасерка и Циннаризина, поскольку последний ослабляет терапевтический эффект Бетасерка своей антигистаминной активностью.
Важное место в механизме действия бетагистина принадлежит его прямому воздействию на рецепторы вестибулярного анализатора, поскольку головокружение нередко является результатом неконтролируемых изменений их спонтанной активности. Бетасерк способен снижать как спонтанную активность вестибулярных рецепторов, так и интенсивность вестибулярного нистагма. Следует подчеркнуть, что, в отличие от традиционно применяемых вестибулярных супрессоров (средств, подавляющих активность вестибулярных нейронов первого и второго порядка), Бетасерк не только не оказывает тормозящего действия на развитие вестибулярной компенсации, но в значительной степени стимулирует ее развитие.
Таким образом, Бетасерк ускоряет развитие компенсации вестибулярной дисфункции как периферического, так и центрального уровня поражения, поскольку обладает прямым действием и на рецепторы вестибулярного анализатора, и на вестибулярные ядра.
Бетасерк является лекарственным препаратом, положительное действие которого на вестибулярную компенсацию наиболее изучено и доказано. Впервые препарат Бетасерк был применен в 1962 г. для лечения кластерной головной боли, а в 1965 г. отмечен его положительный эффект при болезни Меньера. В настоящее время Бетасерк является средством выбора для базисной терапии болезни Меньера, а также других форм вестибулярной дисфункции сосудистого генеза. Вестибулярные расстройства у больных гипертонической болезнью являются следствием морфологических изменений в сосудах, снабжающих вестибулярный анализатор, и ухудшения микроциркуляции в этих областях в результате нарушения реологических свойств крови. Эти изменения плохо корригируются современными вазоактивными препаратами, поэтому в лечении вестибулярной дисфункции центральное место должны занимать средства, улучшающие компенсаторные возможности вестибулярного анализатора и обеспечивающие его нормальную функцию в условиях хронической цереброваскулярной недостаточности.
Клиническая эффективность Бетасерка при различных формах острой вестибулярной дисфункции подтверждается многочисленными рандомизированными двойными слепыми плацебо-контролируемыми исследованиями, удовлетворяющими требованиям доказательной медицины (A.?J.?Fischer, L. W. M. van Elferen, 1985; W.?J.?Oosterveld et al., 1989 и др.). Многолетний опыт применения препарата свидетельствует о его высокой эффективности при различных заболеваниях: при болезни Меньера, вертебро-базилярной недостаточности, после травм головного мозга, при дисциркуляторной энцефалопатии, вестибулярном нейроните, лабиринтитах, возрастных нарушениях равновесия (в том числе при подкорковом синдроме), мигрени, после нейрохирургических операций, операций на ухе.
Терапевтическая доза препарата составляет 48 мг в сутки, длительность курса лечения должна быть не менее двух месяцев.
Бетасерк не вызывает выраженных побочных эффектов, в редких случаях возникают легкие диспептические явления, кожные аллергические реакции и головная боль. Бетасерк противопоказан при индивидуальной повышенной чувствительности к препарату, также необходимо соблюдать осторожность при феохромоцитоме, обострении язвенной болезни желудка и двенадцатиперстной кишки, бронхиальной астме. Хотя экспериментальные исследования не обнаружили тератогенного эффекта Бетасерка, его назначение при беременности и лактации оправдано только в исключительных случаях. В отличие от других вестибулолитических средств препарат не замедляет психомоторные реакции и может назначаться пациентам, деятельность которых связана с повышенным вниманием, в частности, с управлением транспортными средствами.
Таким образом, головокружение может быть симптомом различных заболеваний, встречающихся в повседневной практике врача-терапевта. Знание основных проявлений вестибулярной дисфункции дает возможность составить правильный алгоритм диагностических и лечебных мероприятий и выбрать адекватную тактику лечения больного.
Литература
Афанасьева С.?А., Горбачева Ф.?Е., Натяжкина Г.?М. Изолированное системное головокружение: патогенез и эффективность бетасерка //Неврологич. журн. 2003. № 4.
Бабияк В.?И., Гофман В.?Р., Накатис Я.?А. Нейрооториноларингология. СПб: «Гиппократ», 2002. 726 с.
Храппо Н.?С. Причинные факторы, патогенез, классификация клинических форм вестибулярной дисфункции; принципы лечения // Российская оторинолар. 2009. № 5. С. 119–129.
Верещагин Н.?В. Недостаточность кровообращения в вертебрально-базилярной системе // Consilium medicum. 2001. Прилож. С. 11–15.
Fischer A.?J., van Elferen L.?W.?M. Betahistine in the treatment of paroxysmal attacks of vertigo: a double blind trial // J.?Drug. Ther. Res. 1985. Vol. 10. P. 933–937.
Lacour M., Tighilet B. Vestibular compensation in the cat: the role of histaminergic system // Acta Oto-laringol. (Stockh.). 2000. Suppl. 544. P. 15–18.
Legent F., Calais D., Cellier D. Recurrent paroxysmal vertigo and Serc: controlled clinical trials // Concours. Med. 1988. Vol. 29. P. 342–350.
Oosterveld W.?J., Blijieven W., van Elferen L.?W.?M. Betahistine versus placebo in paroxysmal vertigo: a doubleblind trial // J.?Drug. Ther. Res. 1989. Vol. 14. P. 122–126.
Н. В. Бойко, доктор медицинских наук
РостГМУ, Ростов-на-Дону
Контактная информация об авторе для переписки: nvboiko@gmail.ru
Купить номер с этой статьей в pdf
Источник
В статье представлены данные о клиническом течении заболеваний, сопровождающихся вестибулярным головокружением, принципах постановки диагноза, дифференциальной диагностике. Результаты научных исследований подтверждают эффективность клинического применения препарата Вертигохель при головокружении.
Головокружение — одна из наиболее частых причин обращения к врачам разных специальностей. Так, при опросе более 20 тыс. человек в возрасте от 18 до 64 лет выяснилось, что за месяц более 20% испытали головокружение, из них свыше 30% страдали головокружением на протяжении более 5 лет [1]. В среднем около четверти населения Земли страдают головокружением [2].
Дифференциальная диагностика
Наиболее часто встречающиеся случаи системного головокружения можно разделить на три группы:
головокружение, сопровождающееся тугоухостью;
головокружение, не сопровождающееся тугоухостью;
головокружение с центральными неврологическими симптомами [3].
При возникновении острого вращательного головокружения важно исключить жизнеугрожающие состояния — нарушения мозгового кровообращения в вертебрально-базилярной артериальной системе, симптомы которого варьируют и зависят от того, какая артерия окклюзирована. У пациентов с поражением в бассейне нижней мозжечковой артерии изолированное вращательное головокружение с флюктуирующим снижением слуха и/или ушным шумом, имитирующее приступ болезни Меньера, может отмечаться за 1–10 дней до развития инфаркта мозга. При инсульте в бассейне вертебрально-базилярной артериальной системы головокружение сочетается с другими неврологическими симптомами, однако небольшой очаг в области узелка или клочка мозжечка, в зоне выхода корешка VIII нерва между мостом и продолговатым мозгом и/или вестибулярных ядер может вызвать изолированное головокружение без сопутствующих проявлений. Реже подобная симптоматика встречается при поражении дорзальной инсулярной коры клочка, при этом фиксируется взгляд-индуцированный нистагм [4].
В зависимости от уровня поражения вестибулярного анализатора выделяют периферическое и центральное головокружение, для дифференциальной диагностики которых в последние годы рекомендуется проведение пробы Хальмаге (тест поворота головы) и теста встряхивания
головы [5].
Сочетание отрицательной пробы Хальмаге, вертикального косоглазия (skew deviation), меняющего направление нистагма и нарушение плавного слежения по вертикали позволяет с 100% чувствительностью и 90% специфичностью диагностировать нарушение мозгового кровообращения в стволе мозга. Тест поворота головы значим при поражении в бассейне задней мозжечковой артерии, однако имеет ограничения и может быть положительным при закупорке передней мозжечковой артерии с формированием очага в области клочка мозжечка, в вестибулярных ядрах или зоне выхода VIII нерва [6–9].
Центральное вестибулярное головокружение возникает при повреждении связи с вестибулярными ядрами в стволе мозга, нарушении связей с мозжечком, медиальным продольным пучком, с глазодвигательными ядрами и их собственными связями, нарушении вестибулоспинальных и вестибулоретикулярных связей (тракта), а также связей с корой головного мозга [10]. Ощущение толчка вперед, назад, в стороны (пропульсия, ретропульсия, латеропульсия) с высокой долей вероятности указывает на поражение ствола мозга. Диплопия, дизартрия, потеря чувствительности, парезы, сопутствующие головокружению, характерны для повреждения задней черепной ямки (включая ишемию), базилярной мигрени. Наиболее частые признаки центрального поражения вестибулярной системы, обладающие высокой специфичностью, но низкой чувствительностью [11]:
вертикальный нистагм;
нистагм, меняющий направление;
атипичный нистагм (особенно направленный вниз) в тесте встряхивания головы;
асимметричная глазодвигательная дисфункция;
выраженная постуральная неустойчивость с падениями.
Периферическое вестибулярное головокружение
возникает при поражении сенсорных элементов ампулярного аппарата и преддверия, вестибулярного ганглия и нервных проводников ствола мозга [10] и характеризуется приступообразным течением, вариабельной интенсивностью, сопровождается атаксией и вегетативными проявлениями. При остром начале пациенты ощущают движение предметов в сторону более активно работающего лабиринта, в эту же сторону направлен и нистагм — спонтанный нистагм регулярный, клонический, горизонтальный или горизонтально-ротаторный, разной интенсивности и степени, ассоциированный с гармоничным отклонением туловища и рук в сторону медленного компонента. Отмечается положительное влияние изменения положения головы (в сторону медленного компонента нистагма). Как правило, периферическое вестибулярное головокружение — процесс односторонний и сопровождается нарушением слуховой функции на стороне поражения [12], однако при ряде заболеваний, наиболее ярко отражающих истинную клиническую картину периферического вестибулярного синдрома (доброкачественное пароксизмальное позиционное головокружение, вестибулярный нейронит и в первое время при вестибулярной форме болезни Меньера), слух остается интактным.
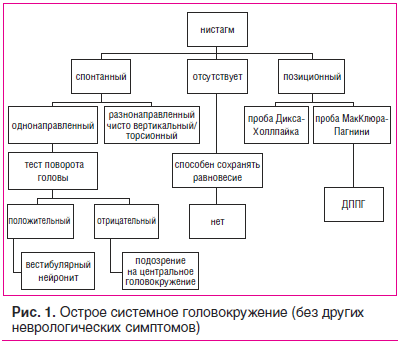
Для экспресс-диагностики вращательного головокружения врачу целесообразно использовать схему «Острое системное головокружение (без других неврологических симптомов)», представленную на рис. 1 [13].
Острый периферический вестибулярный синдром при вестибулярном нейроните и лабиринтите определяется внезапно возникающим приступом интенсивного системного головокружения, нередко с тошнотой, рвотой, гипергидрозом, побледнением кожных покровов. Как правило, возникновению симптомов предшествует вирусное заболевание. При этих заболеваниях головокружение начинается постепенно, усиливается в течение нескольких часов, а затем сохраняется в легкой форме в последующие несколько дней или недель. Головокружение сохраняется и в покое, но субъективно может усиливаться при изменении положения тела [14]. При лабиринтите возможны снижение слуха и ушной шум.
Болезнь Меньера — негнойное заболевание внутреннего уха, характеризующееся увеличением объема эндолимфы (лабиринтной жидкости) и повышением внутрилабиринтного давления, в результате чего возникают рецидивирующие приступы прогрессирующей глухоты (чаще односторонней), шума в ушах, системного головокружения, нарушения равновесия и вегетативных расстройств. При постановке окончательного диагноза «болезнь Меньера», следует придерживаться современного представления об «очевидной» болезни Меньера (табл. 1):![Таблица 1. Дифференциальная диагностика болезни Меньера: расстройства, которые могут проявляться головокружением и слуховыми симптомами [16] Таблица 1. Дифференциальная диагностика болезни Меньера: расстройства, которые могут проявляться головокружением и слуховыми симптомами [16]](https://www.rmj.ru/upload/medialibrary/95f/58-2.png)
два или более самопроизвольных приступов системного головокружения продолжительностью от 20 мин до 12 часов;
подтвержденная аудиологически тугоухость (сенсоневральная) на низких и средних частотах во время или после приступа системного головокружения;
флюктуирующие слуховые симптомы: слух, субъективный шум, ощущение полноты в ухе;
отсутствие иных причин системного головокружения [15].
При болезни Меньера в межприступном периоде показано комплексное лечение (поддерживающая терапия), предотвращающая развитие или уменьшающая эндолимфатический гидропс: диуретики, вазодилататоры (аналог гистамина — бетагистин в суточной дозе 48 мг в течение 2–3-х месяцев и более), кортикостероиды.
Доброкачественное пароксизмальное позиционное головокружение (ДППГ) — это короткое (как правило, не более минуты) головокружение системного характера с тошнотой, возникающее при изменении положения головы: повороты в кровати, запрокидывание головы назад или наклоны вперед.
Патогенетическим механизмом ДППГ является нарушение целостности отолитовой мембраны макулы утрикулюса, приводящее к попаданию отолитов в один или несколько полукружных каналов — каналолитиаз или к фиксации их на купуле — купулолитиаз.
Эпизоды ДППГ повторяются в течение несколько дней подряд, однако иногда ежедневные и многочисленные приступы головокружения длятся в течение многих лет. При длительном течении заболевания пациенты ограничивают себя в обычных действиях из-за страха вызвать приступ головокружения. Нередко после прекращения ДППГ длительно сохраняется нарушение равновесия, особенно в темноте [17].
Для диагностики этого состояния проводятся специальные позиционные пробы, наиболее часто выполняют тест Дикса — Холлпайка [14]. При ДППГ заднего полукружного канала нистагм вертикально-ротаторный (геотропный), направленный в сторону пораженного уха, и возникающий после короткого латентного периода.
Возникающий при проведении пробы Дикса — Холлпайка агеотропный нистагм, направленный вниз, с невыраженным ротаторным компонентом в сторону больного уха (в данном случае оно находится вверху) свидетельствует о встречающемся наиболее редко ДППГ переднего полукружного канала.
При отрицательной пробе Дикса — Холлпайка рекомендуется проведение теста для латерального (горизонтального) полукружного канала — теста МакКлюра — Пагнини [18].
Предпочтительными и наиболее востребованными для лечения ДППГ при поражении заднего канала считаются маневры (методы) Семонта и Эпле, упражнения Брандта — Дароффа.
Фистула лабиринта (перилимфатическая фистула) характеризуется приступом системного головокружения (осциллопсии), возникающего из-за резкого сильного звука, маневра Вальсальвы или изменения давления в наружном слуховом проходе, но не зависит от изменения положения головы [18]. Для выявления дефекта костного лабиринта, включая дегисценцию верхней стенки переднего полукружного канала, выполняется компьютерная томография височных костей (с высоким разрешением, срезами 0,5–1 мм). При остро возникшей фистуле достаточно эффективно консервативное лечение с обязательным соблюдением постельного режима в течение недели (голова должна быть приподнята) и исключением физических нагрузок еще в течение 1,5–2-х месяцев.
У пациентов с мигренью головокружение является одной из наиболее частых жалоб (9–14%) — так называемая вестибулярная мигрень. Такое головокружение может длиться от нескольких секунд до нескольких дней и при этом не сопровождаться головной болью [19].
В настоящее время приняты следующие критерии диагностики вестибулярной мигрени:
эпизодические вестибулярные симптомы;
мигрень согласно критериям IHS (International Headaches Society);
как минимум два из следующих симптомов мигрени, возникающих в течение приступа головокружения: мигренозная головная боль, светобоязнь, звукобоязнь, зрительная или другая аура;
другие причины вестибулярного головокружения исключены [19].
Лечение
Плановое (профилактическое) лечение вестибулярной мигрени проводится в соответствии с классическими принципами лечения мигрени с использованием бета-блокаторов, антиконвульсантов, трициклических антидепрессантов и селективных ингибиторов захвата серотонина и норадреналина, коэнзима Q, рибофлавина.
Купирование острого вестибулярного синдрома предполагает применение антиэметиков и вестибулярных супрессантов. Длительность использования вестибулярных супрессантов и противорвотных средств ограничивается их способностью замедлять вестибулярную компенсацию и не должна превышать 2–3-х дней [20].
При вестибулярном нейроните и лабиринтите в первые 2–3 сут для купирования проявлений острого вестибулярного криза показано внутримышечное введение вестибулярных супрессантов и противорвотных средств. После прекращения тошноты на 1–3 месяца назначается бетагистин внутрь в суточной дозе 48 мг. В этот же период следует начинать курс вестибулярной реабилитации (гимнастики) по индивидуальной программе. В зависимости от особенностей патогенеза вестибулярного нейронита и лабиринтита назначают соответствующее медикаментозное лечение. Так, при вестибулярном нейроните применяют относительно высокие дозы глюкокортикостероидов, например метилпреднизолон в начальной дозе 100 мг с последующим снижением дозы на 20 мг каждые 3 сут. Лечение лабиринтита может потребовать антибактериальных или противовирусных препаратов, в зависимости от возбудителя. Кроме того, при лабиринтите в некоторых случаях прибегают к хирургическому лечению. При лабиринтите, в отличие от вестибулярного нейронита, пациенты зачастую нуждаются в последующей слуховой реабилитации.
Более полувека в мировой медицинской практике в терапии головокружения различного генеза используется препарат Вертигохель® (Vertigoheel®) немецкой фармацевтической компании Heel [21].
В 2005 г. проведен метаанализ результатов двух рандомизированных контролируемых исследований и двух неинтервенционных исследований эффективности и переносимости препарата Вертигохель® в сравнении с препаратами выбора при головокружении. Всего в исследованиях приняли участие 1388 пациентов, из которых 635 получали терапию препаратом Вертигохель®, а 753 — препаратом сравнения (бетагистин, дименгидринат или экстракт гинкго билоба). Препарат Вертигохель® был признан эквивалентным всем исследуемым препаратам сравнения по всем трем рассмотренным критериям эффективности (снижению числа ежедневных приступов головокружения, их продолжительности и интенсивности) [22].
В 2001 г. в референтном контролируемом когортном исследовании на 774 пациентах с головокружением различного генеза оценивалась эффективность и переносимость препарата Вертигохель® в сравнении с дименгидринатом. Среднее число приступов, их интенсивность и продолжительность достоверно снизились в обеих группах. К концу курса лечения у пациентов также купировались и сопутствующие симптомы: тошнота, рвота, повышенное потоотделение. Общий результат терапии был оценен как хороший и отличный в 88% случаев в группе препарата Вертигохель® и в 87% случаев в группе дименгидрината. Переносимость была оценена как хорошая и отличная в 99% случаев в группе препарата Вертигохель® и в 98% случаев в группе дименгидрината [23].
В период с 2009 г. по 2015 г. под наблюдением в нашем Центре находились 89 пациентов в возрасте от 18 до 42 лет (53 женщины и 36 мужчин) с периферическим вестибулярным головокружением, при возникновении острого вестибулярного головокружения и тошноты получавших Вертигохель® по 10 капель каждые 15 мин (не более 2-х часов подряд) или дименгидринат по 50–100 мг (при необходимости каждые 4 часа, но не больше 400 мг/сут). Все пациенты получали оба препарата, но в разные временные промежутки. Большинство пациентов (83 человека — 93%) оценили высокую эффективность обоих средств (как хорошую или отличную), однако все пациенты (89 человек — 100%) отметили лучшую переносимость препарата Вертигохель®, который не вызывал заторможенности и сонливости, характерных для дименгидрината [24].
Таким образом, можно рекомендовать применение препарата Вертигохель® пациентам для купирования острого вестибулярного криза в домашних условиях, поскольку при высокой эффективности препарат характеризуется хорошей переносимостью. Кроме того, Вертигохель® не вступает во взаимодействие с другими лекарственными средствами, что особенно важно для лечения пациентов со смешанным головокружением или полиморбидностью.
Источник


