Головокружение визуально аналоговая шкала
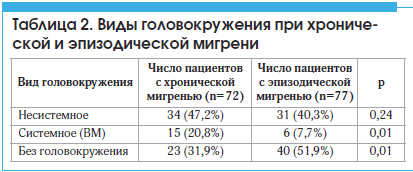
Визуальная аналоговая шкала боли (ВАШ)
Всем хорошего дня. Мы с вами в последнее время очень часто говорим о ремиссии, снижении активности болезни, об активности в общем, индексах активности и тд.
Сегодня и завтра поговорим о том, как эту активность измерить и как результат трактовать. Разберём на примере ревматоидного артрита, если интересуют и другие индексы активности — только сообщите.
Итак, сегодня разберём шкалу боли, которой часто пользуются ревматологи и которая используется для расчёта индексов активности болезни. Шкалы оценки боли предназначены для определения интенсивности болевого синдрома (при любых болезнях). Эти шкалы позволяют оценить субъективные болевые ощущения, которые испытывает пациент боли в момент исследования. Визуальная аналоговая шкала (ВАШ, Visual Analogue Scale, VAS) была предложена Huskisson в 1974 году.
Этот метод субъективной оценки боли заключается в том, что пациента просят отметить на неградуированной линии длиной 10 см точку, которая соответствует степени выраженности боли. Левая граница линии соответствует определению «боли нет совсем», правая — «самая интенсивная боль, какую можно себе представить». Как правило, используется бумажная, картонная или пластмассовая линейка длиной 10 см. С обратной стороны линейки нанесены сантиметровые деления, по которым врач отмечает полученное значение и заносит в историю болезни или амбулаторную карту. Также с целью оценки интенсивности боли можно использовать и модифицированную визуально-аналоговую шкалу, в которой интенсивность боли определяется также различными оттенками цветов.
К безусловным преимуществам этой шкалы относятся ее простота и удобство, возможность контролировать эффективность терапии.
При динамической оценке объективным и существенным является отличие значения по ВАШ от предыдущего более чем на 13 мм.
- Недостатком ВАШ является ее одномерность, т. е. по этой шкале больной отмечает лишь интенсивность боли.
- Эмоциональная составляющая болевого синдрома вносит существенные погрешности в показатель ВАШ.
- Субъективность ВАШ является и основным же ее недостатком. Пациент, преследуя свои цели, может намеренно занижать или завышать значения. Когда? Например, пациент не хочет обижать (напрягать, беспокоить) своего врача, и даже в отсутствии результата и сохранении болевого синдрома на том же уровне занижает значение. Да, бывают и такие) Или же пациент желает получить инвалидность, хочет стать кандидатом на дорогостоящее лечение и тд, и специально ставит оценку значительно выше предыдущего результата. Ну и не стоит забывать, что мы все разные: кто-то будет ходить терпеть да ещё и улыбаться, а кто-то с такой же болью даже с кровати встать не сможет.
Плюс врачу тоже надо быть внимательным и активно коммуницировать (нет, не давить. ) с пациентом. Например, предлагать ему варианты для сравнения. Скажем, в кабинет довольно бодро заходит женщина, но по шкале ставит 10 из 10, все это сопровождая рассказом о том, как ужасно она себя чувствует. Спрашиваешь: «Вы рожали? Так же больно?». «Ой, ну нет, доктор, вы что, когда рожала, думала, что умру». После этого значение снижается до 5. Именно поэтому ВАШ является лишь одним из инструментов для вычисления индекса активности самим врачом, который использует уже объективные методы оценки состояния пациента. Тут можно стоит вспомнить доктора Хауса и его железное «Все врут», но мы с вами люди воспитанные и не будем так категорично выражаться????
. Напоследок хочется сказать только одно: пожалуйста , будьте честны со своим врачом. Если вам стало лучше — говорите об этом, если стало хуже — опять-таки скажите врачу об этом. Не стоит специально что-то подделывать или скрывать. Если врач вас не слышит, не хочет слышать — значит, просто это не ваш врач. Завтра обсудим DAS-28 и что считать ремиссией.
Использованные источники: www.revmadoctor.ru
ВАС МОЖЕТ ЗАИНТЕРЕСОВАТЬ :
Беременность головокружение всд
Беременность 3 дня головокружение
Жидкий стул и головокружение при беременности
Плохое самочувствие при беременности головокружения
Головокружения при мигрени
О статье
Авторы: Иванова Т.А. (ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), Москва), Гусева А.Л. (ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» МЗ РФ, Москва), Филатова Е.Г. (ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), Москва)
Головокружение при мигрени встречается чаще, чем в популяции и среди пациентов, предъявляющих другие жалобы, в частности на головную боль напряжения. Распространенность головокружения составляет около 20–30%, с доминированием у женщин. Клиническая и патофизиологическая взаимосвязь мигрени и головокружения до сих пор остается неясной, подходы к лечению вестибулярной мигрени (ВМ) не разработаны.
Цель исследования: определить характер головокружения у пациентов, страдающих мигренью с аурой и без ауры, и патогенетических механизмов их связи.
Материал и методы: в исследование было включено 152 пациента с мигренью с аурой (24 чел.) и без ауры (128 чел.). Всем пациентам проводилось клиническое неврологическое исследование, а пациентам с головокружением в анамнезе проводилось дополнительно комплексное отоневрологическое исследование: видеонистагмография, видеоимпульсный тест, калорическая проба, диагностические позиционные маневры, тональная пороговая аудиометрия. Анкетное исследование пациентов с мигренью, предъявлявших жалобы на головокружение, включало: отоневрологический опросник, шкалу оценки головокружения.
Результаты : 58,6% пациентов с мигренью предъявляли жалобы на головокружение, 2,6% имели признаки периферической вестибулопатии, у 13,8% была диагностирована вестибулярная мигрень (ВМ), 42,1% страдали несистемным головокружением. ВМ чаще отмечалась при хронической мигрени (ХМ), и топирамат оказывал хорошее терапевтическое воздействие как на частоту головной боли, так и на головокружение. Выявлялся также позиционный характер головокружения при ВМ по DHI.
Заключение : головокружение при ВМ носит смешанный характер, в патогенезе заболевания принимают участие как центральные механизмы в виде центральной сенситизации, так и периферические, обусловленные активацией тригемино-васкулярной системы. У большинства пациентов головокружение при ВМ носит позиционный характер. В статье показано, что антиконвульсант топирамат является препаратом выбора с доказанной эффективностью при мигрени.
Ключевые слова: мигрень, вестибулярная мигрень, головокружение, топирамат.
Для цитирования: Иванова Т.А., Гусева А.Л., Филатова Е.Г. Головокружения при мигрени // РМЖ. 2017. №9. С. 602-606
Migraine vertigo Ivanova T.A. 1 , Guseva A.L. 2 , Filatova E.G. 1 1 First Moscow State Medical University named after I.M. Sechenov 2 Russian National Research Medical University named after N.I. Pirogov, Moscow Migraine vertigo is common in the population and among the patients with other complaints, in particular the headache of tension. The prevalence of vertigo is about 20-30%, with dominance in women. The clinical and pathophysiological connection between migraine and vertigo is still unclear, approaches to the treatment of vestibular migraine (VM) have not been developed.
Aim : to determine the nature of vertigo in patients with migraine with aura and without aura, and pathogenetic mechanisms of their connection.
Patients and methods: 152 patients having migraine with aura (24 people) and without aura (128 people) were included into the study. All patients underwent a clinical neurological examination, and patients with a history of vertigo had an additional comprehensive otoneurological examination: videoistagmography, video pulse test, caloric assay, diagnostic positional maneuvers, and tone threshold audiometry. A questionnaire study of patients with migraine, who complained of dizziness, included: otoneurological questionnaire; and Dizziness Assessment Rating Scale.
Results : 58.6% of patients with migraine complained of vertigo, 2.6% had signs of peripheral vestibulopathy, 13.8% had vestibular migraine (VM), 42.1% suffered from non-rotary vertigo. VM was more often observed with chronic migraine (CM) and topiramate had a good therapeutic effect, both on the incidence of headache and on vertigo. There was also a positional character of vertigo with VM on DHI.
Conclusion: vertigo with VM has a mixed character, in the pathogenesis of which both central mechanisms in the form of central sensitization, and peripheral ones, caused by activation of the trigemino-vascular system are involved. In most patients, vertigo with VM is positional. The article shows that anticonvulsant topiramate is the drug of choice with proven effectiveness in migraine headaches.
Key words: migraine, vestibular migraine, vertigo, topiramate
For citation: Ivanova T.A., Guseva A.L., Filatova E.G. Migraine vertigo // RMJ. 2017. № 9. P. 602–606.
Статья посвящена проблеме головокружения при мигрени
Актуальность
Материал и методы
Статья посвящена возможностям применения противотревожной терапии у пациентов с «гипертони.
Представлены новые возможности лечения вегетативной дисфункции
Использованные источники: www.rmj.ru
ВАС МОЖЕТ ЗАИНТЕРЕСОВАТЬ :
Беременность головокружение всд
Беременность 3 дня головокружение
С чем связано головокружение при беременности
Чем лечить головокружение при беременности
Диагноз боли, оценка состояния пациента и мониторинг
Боль — субъективное явление, поэтому с трудом поддается объективной оценке.
Исчерпывающая оценка боли, включая как субъективные, так и объективные данные, является существенной для определения объема необходимого вмешательства.
Известно, что методы доказательной медицины, в частности, аналитические мета-анализы рандомизированных исследований, позволяют получать интегрированные оценки эффективности используемых в различных клиниках диагностических программ.
Однако на практике оказывается, что, несмотря на обилие разработанных тестов, во-первых, до сих пор не существует унифицированного метода диагностики, который бы позволил получать точку отсчета при проведении исчерпывающего анализа; во-вторых, крайне затруднительно сравнивать методологию диагностики боли при различных клинических состояниях (диагностику послеоперационной боли и онкологической и т.п.); в-третьих, необходимо выделять и рассматривать двe абсолютно самостоятельные программы оценки острой и хронической боли; в-четвертых, не удается проследить динамику пересмотра диагностических тестов при проведении повторных клинических испытаний лекарственных препаратов, используемых при обезболивании; и, наконец, в целях конвергенции данных по использованию различных методов тестирования требуется введение дополнительной обобщающей величины.
Тем не менее, минимальный объем элементарного диагностического тестирования достаточно стандартизован и может быть использован для оценки всех видов боли независимо от вызвавшей ее причины. Он включает несколько разделов согласно многофакторной концептуальной модели боли.
Для начала необходимо уделить особое внимание описанию боли пациентом. Это способно дать важную информацию относительно причин ее возникновения и интенсивности, привести к распознаванию ее источника. Хорошим примером является «ощущение жара, жжения», описываемое пациентами с герпетической невралгией. Нервная или нейропатическая боль обычно описывается как «пекущая, жгучая, ошпаривающая, обжигающая».
Пациенту трудно найти нужные слова и выражения, описать свои ощущения. Он пытается создать у врача определенное эмоциональное состояние, подобное тому, которое он испытывает, добиться сопереживания. Необходимо позволять пациентам быть специфичными в описании своих ощущений настолько, насколько это возможно, относясь с уважением и вниманием к описанию характера и локализации боли.
С целью облегчения общения врача и пациента, объективизации переживаний последнего, дифференциально-диагностического и терапевтического сопоставления данных были созданы опросники, состоящие из наборов стандартных вербальных дескрипторов, наиболее общих для всех пациентов.
Стандартным методом обследования за рубежом является «МакГилловский опросник боли» (McGill Pain Questionnaire — MPQ), использующий вербальные характеристики сенсорных, аффективных, и моторно-мотивационных компонентов боли, ранжированных по пяти категориям интенсивности (табл. 3).
Первый класс — дескрипторы сенсорных характеристик
Использованные источники: medbe.ru
ВАС МОЖЕТ ЗАИНТЕРЕСОВАТЬ :
Беременность головокружение всд
Головокружение беременность или пмс
Головокружение во сне при беременности
Головокружение и удушье при беременности
Диагностика боли у онкологического пациента
Для диагностики болевого синдрома у онкологических пациентов из этических соображений принято применять только неинвазивные методы. В начале необходимо изучить анамнез боли (давность, интенсивность, локализация, тип, факторы, усиливающие или уменьшающие боль; время возникновения боли в течение дня, применявшиеся ранее анальгетики и их дозы и эффективность). В дальнейшем следует провести клинический осмотр пациента с целью оценки характера и распространенность онкологического процесса; изучить физический, неврологический и психический статус пациента. Необходимо ознакомиться с данными клинико-лабораторных методов исследования (клинический и биохимический анализ крови, анализ мочи), что важно для выбора наиболее безопасных для данного пациента комплекса анальгетиков и адъювантных средств (АД, ЧСС, ЭКГ, УЗИ, рентгенография и др.).
Оценку интенсивности хронического болевого синдрома проводят с помощью шкалы вербальных (словесных) оценок (ШВО), визуально аналоговой шкалы (ВАШ), болевых опросников (McGill Pain Questionaire и др.). Наиболее простой и удобной для клинического применения является 5-балльная ШВО, которая заполняется врачом со слов пациента:
0 баллов — боли нет,
1 балл — слабая боль,
2 балла — боль умеренная,
3 балла — боль сильная,
4 балла — нестерпимая, самая сильная боль.
Нередко применяют визуально-аналоговую шкалу (ВАШ) интенсивности боли от 0 до 100%, которую предлагают пациенту, и он сам отмечает на ней степень своих болевых ощущений.
Эти шкалы позволяют количественно оценить динамику хронического болевого синдрома в процессе лечения.
Оценка качества жизни онкологического пациента может быть достаточно объективно проведена по 5-ти балльной шкале физической активности:
- 1 балл — нормальная физическая активность,
- 2 балла — незначительно снижена, больной способен самостоятельно посещать врача,
- 3 балла — умеренно снижена (постельный режим менее 50% дневного времени,
- 4 балла — значительно снижена (постельный режим более 50% дневного времени),
- 5 баллов — минимальная (полный постельный режим).
Для оценки общего состояния онкологического больного применяется шкала оценки качества жизни по Карнофски, где динамику степени активности пациента измеряют в процентах:
Для более детальной оценки применяется целый комплекс критериев, рекомендуемый Международной Ассоциацией по изучению боли (IASP, 1994), включающий следующие параметры:
- общее физическое состояние
- функциональная активность
- социальная активность,
- способность к самообслуживанию
- коммуникабельность, поведение в семье
- духовность
- удовлетворенность лечением
- планы на будущее
- сексуальные функции
- профессиональная деятельность
Для оценки переносимости анальгетической терапии учитывают появление побочного эффекта, вызванного тем или иным препаратом (сонливость, сухость во рту, головокружение, головная боль и др.) и степень его выраженности по 3-х балльной шкале:
0 — нет побочных эффектов,
1 — слабо выражен,
2 — умеренно выражен,
3 — сильно выражен.
При этом следует помнить, что у больных с распространенными формами опухолей могут присутствовать симптомы, сходные с побочным действием многих анальгетиков (тошнота, сухость во рту, головокружение, слабость), поэтому важно начать оценку исходного статуса до начала анальгетической терапии или ее коррекции.
Для углубленной оценки боли в специальных научных исследованиях применяются нейрофизиологические методы (регистрация вызванных понтенциалов, ноцицептивный флексорный рефлекс, исследование динамики условно-негативной волны, сенсометрия, электроэнцефалография), проводится определение плазменного уровня стресс-факторов (кортизола, соматотропного гормона, глюкозы, бета-эндорфина и др.). Последнее время стало возможным объективизировать уровень болевых ощущений по данным активности различных отделов мозга с помощью позитронно-эмиссионной томографии. Но применение этих методов их в ежедневной практике ограничено из-за их инвазивности и высокой стоимости.
Академический интерес представляет тест на опиатную зависимость с налоксоном, который проводят в специализированных клиниках с согласия пациента при длительной (свыше месяца) терапии опиоидными анальгетиками. В обычной практике он не применяется, поскольку может привести к устранению анальгезии и развитию острого абстинентного синдрома.
На основании данных диагностики устанавливается причина, тип, интенсивность хронического болевого синдрома, локализация боли, сопутствующие осложнения и возможные психические нарушения. На последующих этапах наблюдения и терапии необходимо проводить повторную оценку эффективности обезболивания. При этом достигается максимальная индивидуализация болевого синдрома, отслеживаются возможные побочные эффекты применяемых анальгетиков и динамика состояния пациента.
Опрос о бремени болезни среди пациентов
Помогите докторам узнать о мигрени больше. Ваше мнение и ощущения очень важны, чтобы мы могли лучше помогать вам справляться с мигренью!
Использованные источники: www.paininfo.ru
загрузка…
Источник
Актуальность
Мигрень и головокружение являются самыми распространенными расстройствами в популяции, нередко их сочетание наблюдается у одного пациента. Однако недавние эпидемиологические исследования показали, что сочетание мигрени и головокружения встречается чаще, чем этого можно было бы ожидать от случайного совпадения двух весьма распространенных симптомов [1].
Метаанализ нескольких крупных популяционных исследований, включавших более 35 461 000 человек в возрасте 18–65 лет, показал, что распространенность мигрени составляет около 12%, с соотношением мужчины/женщины, равным 0,4 [2]. Распространенность головокружения составляет около 20–30%, также с доминированием у женщин (соотношение мужчины/женщины равно 0,37), а пациенты с коморбидностью этих состояний составляют около 4% в общей популяции. Около 73% пациентов с установленным диагнозом «мигрень» жалуются на головокружение. Крупное эпидемиологическое популяционное исследование (Германия) выявило, что распространенность мигрени среди населения – около 14%, а распространенность головокружения – 7%. Вероятность их случайного совпадения составляет около 1%, что дает возможность сделать вывод о наличии в анамнезе взрослого населения как мигрени, так и головокружения примерно в 3 раза более частом, чем это могло бы быть при простом совпадении, а именно у 3,2% людей в популяции [3]. Существуют и другие данные, свидетельствующие о неслучайном сочетании (коморбидности) мигрени и головокружения. Около 61% пациентов с вестибулярными нарушениями страдают мигренью. Проведены исследования, где описано наличие головокружения у 47,5% пациентов, страдающих мигренью с интенсивностью головной боли 7 баллов и более по визуальной аналоговой шкале (ВАШ), где 0 баллов – отсутствие боли, 10 баллов – невыносимая головная боль [4].
Эпидемиологические исследования ассоциаций мигрени и головокружения подчеркивают двунаправленный характер взаимоотношений между ними. С одной стороны, мигрень чаще встречается среди пациентов с головокружением. Так, мигрень, полностью соответствующая критериям МКГБ-3, бета-версия, распространена среди пациентов, страдающих головокружением, в 1,6 раза чаще (38%), чем среди пациентов, обратившихся за медицинской помощью с другими жалобами (24%). Y. Cha et al. [5] обнаружили, что из 208 пациентов с доброкачественным рецидивирующим головокружением 87% страдали мигренью, причем 70% из них отвечали диагностическим критериям вестибулярной мигрени, предложенным H. Neuhauser et al. [6]. По данным другого исследования, пациенты из группы с доброкачественным рецидивирующим головокружением страдали мигренью в 6 раз чаще, чем пациенты контрольной группы, сопоставимой по полу и возрасту (61 и 10% соответственно) [1]. C. Rassekh и L. Harker выявили, что распространенность мигрени среди пациентов с доброкачественным рецидивирующим головокружением составляет 81%, тогда как среди пациентов с болезнью Меньера – 22% [7]. При этом у пациентов с головокружением мигрень вызывает сильную дезадаптацию, часто сопровождаясь симптомами депрессии. В то же время мигрень нередко сосуществует с некоторыми периферическими вестибулопатиями, такими как болезнь Меньера и доброкачественное пароксизмальное позиционное головокружение, так что часть случаев сочетания мигрени и головокружения, по-видимому, может быть объяснена этим обстоятельством [1, 8, 9].
В медицинской литературе под головокружением понимают широкий спектр расстройств от ощущения мнимого вращения или движения окружающих предметов (истинное, или системное головокружение – vertigo) до нарушения равновесия (несистемное головокружение – dizziness). Более того, многочисленные исследования показали, что у больных с мигренью во время приступа головной боли нередко возникают те или иные вестибулярные нарушения, что послужило поводом для обсуждения особой формы мигрени – вестибулярной мигрени (ВМ) или мигрень-ассоциированного головокружения.
Первые описания пациентов, у которых головокружение и головная боль возникали как единое состояние, содержатся в трудах Аретеуса из Каппадокии (100 г. до н. э.). По мере накопления данных для определения этого сочетания разные авторы стали одновременно использовать различные термины: «вестибулярная мигрень», «мигрень-ассоциированное головокружение», «доброкачественное рецидивирующее головокружение», «связанная с мигренью вестибулопатия» и др. Первое описание ВМ было сделано R. Slater в 1979 г. [1].
Коморбидность с головокружением характерна в большей степени именно для мигрени, а не для других форм головной боли: распространенность головокружения среди пациентов с головной болью напряжения составляет 8%, а среди пациентов с мигренью – 27% [1]. По другим данным, на головокружение жалуются 30% пациентов с головной болью напряжения и 55% пациентов с мигренью. При этом несистемное головокружение возникает у 28–30% пациентов с мигренью, а системное – у 25–26% [10]. Известно, что как мигрень, так и головокружение часто сопровождаются тревожными расстройствами. Однако тревожные расстройства вряд ли могут быть причиной всего разнообразия вестибулярных симптомов при мигрени.
Международная ассоциация головной боли совместно с Обществом Барани составили диагностические критерии для ВМ, которые были отражены в приложении к новой бета-версии МКГБ-3 Международной классификации головной боли [11] (табл. 1).
Эти диагностические критерии разработаны для того, чтобы продолжить дальнейшие исследования ВМ, включая терапевтические подходы к ее лечению. По данным некоторых исследований, распространенность ВМ в общей популяции составляет 1%, а само заболевание занимает 1-е место среди вестибулопатий центрального генеза и 2–е место среди заболеваний, сопровождающихся вращательным головокружением [12, 13]. Дебютировать ВМ может в любом возрасте. Женщины ей подвержены чаще, чем мужчины.
Несмотря на многочисленные эпидемиологические исследования, демонстрирующие тесную взаимосвязь между мигренью и головокружением, остается ряд спорных вопросов в отношении ВМ как самостоятельного заболевания – в первую очередь вопросы терминологии и возможности рассмотрения головокружения в качестве главного и зачастую единственного проявления приступа мигрени. ВМ часто начинается через несколько лет после появления обычной мигрени и имеет разнообразную клиническую картину. У пациентов с ВМ при проведении неврологического и отоневрологического обследования в подавляющем большинстве случаев патология не выявляется, а диагноз основывается на анамнезе заболевания. Несмотря на то что, по статистическим данным, пациенты с ВМ составляют 7% от общего количества обращений в клиники головокружений и 9% – в клиники головной боли, это заболевание до сих пор остается редко диагностируемым [14]. На сегодняшний день отсутствуют какие-либо определенные представления о клинической и патофизиологической взаимосвязи между мигренью и головокружением, а также специфические подходы к лечению именно ВМ.
Цель исследования: определить характер головокружения у пациентов, страдающих мигренью с аурой и без ауры, и патогенетические механизмы их связи.
Материал и методы
В исследование включено 152 пациента 18–65 лет, с диагнозом «мигрень с аурой и/или без ауры» согласно МКГБ-3, бета-версия, обратившихся на прием в Клинику головной боли и вегетативных расстройств им. Александра Вейна. Диагноз ВМ ставился на основании критериев Н. Neuhauser [6]. Критериями исключения пациентов из исследования были: 1) возраст моложе 18 и старше 65 лет; 2) неврологические заболевания или заболевания внутренних органов, крови, сопровождающиеся головокружением и нарушением равновесия; 3) центральные и периферические вестибулопатии; 4) психические нарушения, затрудняющие самооценку и заполнение опросников; 5) беременные и кормящие пациентки.
Всем пациентам проводилось клиническое неврологическое исследование, а пациентам с головокружением в анамнезе проводилось дополнительно комплексное отоневрологическое исследование: видеонистагмография, видеоимпульсный тест, калорическая проба, диагностические позиционные маневры, тональная пороговая аудиометрия [15].
Анкетное исследование пациентов с мигренью, предъявлявших жалобы на головокружение, включало: отоневрологический опросник, разработанный специально для пациентов с головокружением, неустойчивостью, проблемами со слухом, для выяснения наличия вестибулопатии, характера головокружения, связи головокружения с головной болью, провоцирующих приступ головокружения факторов, укачивания в анамнезе, а также наличия симптомов вестибулопатии у родственников пациента [16]; шкалу оценки головокружения (Dizziness Handicap Inventory – DHI), разработанную G. Jacobson et al. в 1990 г. [17]. Шкала DHI включает 25 вопросов с тремя вариантами ответов («да», «нет», «иногда»). Ответ «да» оценивался в 4 балла, «иногда» – 2 балла, «нет» – 0 баллов. Таким образом, суммарный балл по DHI может составлять от 0 (нет головокружения) до 100 (очень выраженное головокружение). Считается, что головокружение отсутствует, если суммарный показатель DHI ниже 14 баллов. При сумме баллов от 1 до 30 говорят о легком головокружении, от 31 до 60 – об умеренном, свыше 60 – о выраженном головокружении. DHI имеет 3 подшкалы: функциональную (по ней оценивают, в какой степени головокружение нарушает повседневную активность больного), эмоциональную (в какой степени головокружение нарушает эмоциональное состояние больного) и физикальную (в какой степени движения головы и тела влияют на головокружение). В целом эта шкала позволяет количественно оценить влияние головокружения на физическое и эмоциональное состояние пациента, что особенно важно при динамическом контроле за ходом лечения. Кроме того, для определения выраженности болевого синдрома пациентам предлагалось заполнить анкету ВАШ для оценки интенсивности головной боли.
Для обработки материала использовались параметрический статистический метод – Т-критерий Стьюдента для сравнения переменных, а также непараметрические методы статистики: метод сравнения качественных показателей путем анализа таблиц сопряженности с вычислением критерия Хи-квадрат. Статистически значимыми считались различия при р<0,05.
Результаты
Всего было обследовано 152 пациента, страдающих мигренью с аурой (24 человека) и без ауры (128 человек), согласно критериям МГКБ-3, бета-версия от 2013 г. Средний возраст пациентов составил 39,5±13,1 года, женщин было 122, мужчин – 30. Более половины пациентов – 58,6% (89) – предъявляли жалобы на головокружение, а у 41,4% (63) головокружений не отмечено; 25 (16,4%) пациентов предъявляли жалобы на системное головокружение. У 4-х (2,6%) пациентов с системным головокружением при отоневрологическом осмотре были выявлены признаки периферической вестибулопатии и диагностированы следующие заболевания: вестибулярный нейронит – 1 случай, ДППГ – 2 случая, болезнь Меньера – 1 случай. Эти пациенты были исключены из основной группы. У остальных пациентов с мигренью, предъявлявших жалобы на эпизоды вращательного головокружения, при отоневрологическом обследовании в межприступном периоде клинические признаки периферической или центральной вестибулопатии не выявлены. Эти пациенты – с мигренью и системным головокружением (или ВМ) – составили основную группу исследования (рис. 1).
При анализе клинической симптоматики в основной группе с использованием критериев H. Neuhauser [18] вероятная вестибулярная мигрень (ВВМ) была диагностирована у 5,9% (9) пациентов, достоверная вестибулярная мигрень (ДВМ) – у 7,9% (12). Пациенты предъявляли жалобы на мигренозную головную боль и головокружение системного характера, которое в части случаев возникало на фоне головной боли и провоцировалось мигренозными триггерами. По выраженности головокружения согласно DHI, представленности хронической мигрени и эпизодической мигрени, мигрени с аурой и без ауры, а также по демографическим показателям пациентов с достоверной и вероятной ВМ достоверных отличий не выявлено. В результате проведенного сравнительного анализа пациенты с ВВМ и ДВМ были объединены в основную группу ВМ (мигрени и системного головокружения).
Группу сравнения составили 42,1% (64) пациентов с мигренью и несистемным головокружением. При подробном расспросе о характере головокружения эти пациенты описывали его как ощущение неустойчивости, вращения внутри головы, дереализации, шаткости при ходьбе, качания, тумана в голове и страха упасть.
Согласно критериям МКГБ-3, бета-версия, 72 пациента страдали хронической мигренью, а 77 – эпизодической ее формой. В результате сравнения пациентов с хронической и эпизодической мигренью по полу, возрасту, длительности заболевания, возрасту дебюта мигрени получены статистически достоверные отличия между этими группами только по частоте головной боли (что является основным принципом разделения).
В результате сравнения 2-х групп пациентов с хронической и эпизодической мигренью по представленности различных видов головокружения оказалось, что пациенты с эпизодической мигренью меньше предъявляют жалоб на головокружение по сравнению с пациентами с хронической мигренью: 23 (31,9%) vs 40 (51,9%) (p<0,01). При хронической мигрени системное головокружение наблюдалось чаще, чем при эпизодической мигрени: 15 (20,8%) vs 6 (7,7%) (p<0,01) (табл. 2).
Таким образом, по мере увеличения числа дней с головной болью увеличивается как число пациентов с жалобами на головокружение в целом, так и представленность ВМ.
Сравнение 2-х групп пациентов – с системным (ВМ) и несистемным головокружением – по клинико-демографическим показателям достоверных отличий не выявило (табл. 3).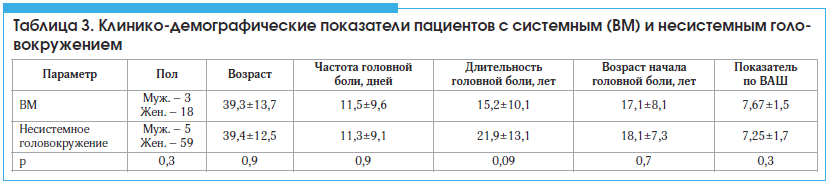
Данные отоневрологического опросника: большая часть пациентов основной группы субъективно в анамнезе отмечали проблемы со слухом: 57,2% (12) vs 35,2% (12) пациентов группы сравнения (p<0,09) (хотя ни у кого из пациентов при обследовании ЛОР-врачом патология не выявлялась); больше чем у половины обследованных пациентов с ВМ головокружение усиливалось при перемене положения головы, т. е. носило позиционный характер – 57,2% (12) vs 29,4% (10) (p<0,05), и беспокоило укачивание в транспорте – 80,95% (17) vs 54,3% (19) (p<0,05). По другим показателям отоневрологического опросника достоверных отличий не выявлено.
При сравнении средних показателей выраженности головокружения по cпециальной шкале (Dizziness handicap inventory) в основной группе пациентов с ВМ и группе сравнения достоверных отличий не получено. Однако при анализе подшкал выявлено статистически достоверное увеличение показателя по шкале DHI P у пациентов с системным головокружением при мигрени: 15,43±5,9 vs 12,28±6,9 соответственно (p<0,05), что указывает на позиционный характер головокружения в группе ВМ. В этой же группе определялась достоверная связь головной боли и головокружения (табл. 4).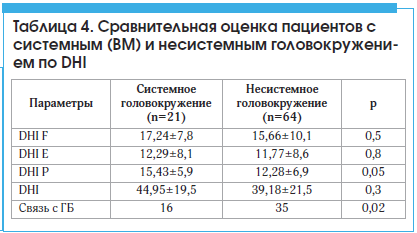
Всем пациентам основной группы с ВМ было проведено профилактическое лечение топираматом: в течение первого месяца осуществлялось постепенное титрование дозы с 25 мг/сут до 100 мг/сут; общая длительность терапии составила 6 мес. Результаты лечения оценивались путем анализа дневников головной боли и динамики шкалы оценки головокружения (ШОГ): 16 пациентов с ВМ показали статистически достоверное уменьшение числа дней с головной болью (11,63±8,5 vs 2,8±1,04, р<0,01), а также числа дней с головокружением (14,88±8,4 vs 2,3±2,4, р<0,01). Суммарный показатель выраженности головокружения по ШОГ уменьшился с умеренно выраженного до слабого (45±17,03 vs 9,3±2,5, р<0,01). Пять пациентов по различным причинам не провели рекомендованной терапии.
Заключение
Больше половины пациентов с мигренью (58,6 %), обратившихся в специализированную клинику, предъявляли жалобы на головокружение, что соответствует данным литературы о коморбидности этих состояний. В отечественной практике под головокружением понимают самые различные состояния. Это не только ощущение вращения, но и неустойчивость, туман в голове, страх упасть, ощущение секундного покачивания и другие, которые собственно головокружением не являются. В связи с этим нами были выделены пациенты с мигренью, предъявлявшие жалобы на ощущение вращательного головокружения, которые составили 13,8%. У 2,6% пациентов при отоневрологическом осмотре выявлена периферическая вестибулопатия, что подтверждает ранее известные данные о ее частом сочетании с мигренью [14]. 42,1% пациентов с мигренью описывали головокружение несистемного характера. На основании критериев МКГБ-3, бета-версия, пациентам с системным головокружением был поставлен диагноз «вестибулярная мигрень».
Нами показано, что системное головокружение (или ВМ) чаще возникает у пациентов с хронической мигренью. На сегодняшний день отсутствуют какие-либо определенные представления о клинической и патофизиологической взаимосвязи между мигренью и головокружением, вместе с тем полученные в нашей работе данные о преимущественно хроническом течении ВМ подтверждают одну из известных теорий о роли центральной сенситизации в вовлечении в патологический процесс центрального отдела вестибулярной системы – вестибулярных ядер и их связей. Для подтверждения ведущей роли центральной сенситизации в качестве основного механизма коморбидной связи мигренозной головной боли и вестибулярных расстройств было проведено лечение пациентов топираматом. Анти-конвульсант топирамат является препаратом выбора с доказанной эффективностью при мигрени [19, 20]. Механизм его действия основан на снижении возбудимости как коры головного мозга, так и сенситизированных тригеминальных афферентов, что приводит к уменьшению выделения из их окончаний вос


