Велафакс боль головная боль
Комментарии
Опубликовано в журнале:
«Лечащий врач» май 2008, № 5, с. 1-5
Н. В. Латышева
Е. Г. Филатова, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва
Хроническая ежедневная головная боль (ХЕГБ) беспокоит пациентов более 15 дней в месяц на протяжении более трех месяцев. ХЕГБ не является самостоятельной нозологической формой, а представляет синдром, включающий различные первичные и вторичные головные боли (ГБ). Распространенность ХЕГБ в популяции составляет примерно 3–5%, а в специализированных клиниках доля пациентов с ежедневной или почти ежедневной ГБ достигает 70–80%. Заболевание обуславливает значительное снижение качества жизни, нарушает социальную активность пациентов и их трудоспособность, а также представляет собой сложную проблему с точки зрения терапии.
Самыми частыми формами ХЕГБ являются хроническая мигрень (ХМ), хроническая ГБ напряжения (ХГБН) и абузусная ГБ. ХЕГБ в большинстве случаев является осложнением длительно существующей эпизодической ГБ и лишь у немногих пациентов с момента своего дебюта принимает ежедневный или почти ежедневный характер.
Среди факторов хронизации ГБ описаны ожирение, женский пол, исходно частая ГБ (более 1 раза в неделю), чрезмерное употребление анальгетических препаратов (более 10 дней в месяц) и эмоциональный стресс. У более чем половины пациентов с ХЕГБ выявляются нарушения сна и расстройства настроения депрессивного и тревожного характера.
Патогенез ХЕГБ в настоящее время изучен недостаточно. Предполагаются два основных механизма, которые могут лежать в основе хронизации разных форм ГБ — сенситизация ноцицептивных структур и снижение активности антиноцицептивных отделов центральной нервной системы (ЦНС).
При мигрени периферическая сенситизация происходит в сенсорных нейронах, иннервирующих внутримозговые сосуды и оболочки. Центральная сенситизация (ЦС) описана в спинномозговом ядре тройничного нерва, куда стекаются импульсы от мозговых оболочек и кожи лица. Многие пациенты испытывают неприятные ощущения во время и между приступами мигрени при бритье, расчесывании волос, ношении очков и украшений. Ощущение боли при воздействии неболевого раздражителя обозначается как аллодиния, которая в настоящее время часто коррелирует с центральной сенситизацией. Различают статическую (от давления или укола) и динамическую (от поглаживания) аллодинию. При дальнейшем течении некупированного приступа мигрени включаются более центральные отделы ноцицептивной системы. Уже при активации таламуса аллодиния становится двусторонней, ее зона может с головы и лица переходить на руку. При эпизодической мигрени в течение 72 часов включаются антиноцицептивные системы, которые приводят к купированию мигренозного приступа.
Со временем признаки ЦС исчезают не полностью после окончания приступа, и постепенно формируется стабильная ЦС, которая поддерживает боль в хроническом состоянии. При этом нейроны в ЦНС становятся слабо или совсем нечувствительными к периферическим воздействиям. На этом этапе терапевтические воздействия должны быть направлены на усиление нисходящих антиноцицептивных влияний — on/off-нейроны в околоводопроводном сером веществе (ОСВ), антиноцицептивная функция которых нарушена при ХЕГБ.
В настоящее время для профилактики ГБ активно используются антидепрессанты. Показано, что анальгетическое действие трициклических антидепрессантов (ТЦА) не зависит от их антидепрессивного действия и обусловлено их сочетанным серотонинергическим и норадреналинергическим действием. В то же время более безопасные селективные ингибиторы обратного захвата серотонина (СИОЗС) недостаточно эффективны в лечении мигрени и ХГБН [21].
Венлафаксин, структурно новый антидепрессант, по химической структуре отличен от ТЦА, однако также угнетает обратный захват серотонина (5-HT) и норадреналина. Кроме того, по сравнению с амитриптилином препарат действует более специфично на эти рецепторы. Венлафаксин облегчает головную боль так же эффективно, как и ТЦА, но вызывает гораздо меньше побочных эффектов. В ходе двойного слепого исследования профилактического эффекта СИОЗС и венлафаксина при мигрени было показано, что процент пациентов, у которых было достигнуто значительное улучшение в группе венлафаксина, превысил этот показатель в группе СИОЗС.
Эффективность венлафаксина неоднократно доказана в исследованиях пациентов с различными формами нейропатической боли: при диабетической полинейропатии, нейропатии после химиотерапевтического лечения и др. Проведен также ряд исследований профилактического действия венлафаксина при хронической мигрени и ХГБН.
Целью настоящей работы явилось изучение феномена ЦС при ХЕГБ, ее роли в хронификации ГБ и эффективности венлафаксина для ее урежения.
Материал. В исследовании приняли участие 69 пациентов с ХЕГБ и 30 пациентов с эпизодической мигренью (ЭМ) в соответствии с критериями ICHD-2, а также 15 участников группы контроля с ГБ не чаще 1 дн./мес. Группа ХЕГБ была представлена пациентами с ХМ, ХГБН и пациентами со смешанными формами ГБ.
Методы исследования. Всем пациентам была предложена анкета для изучения демографических данных, анамнеза и клинической картины головной боли. Кроме того, пациенты заполняли анкету для изучения симптомов аллодинии.
Статическая аллодиния (СА) исследовалась при помощи альгометра в 5 парах симметричных точек на голове и шее (лоб, висок, темя, задняя поверхность шеи, плечо/трапециевидная мышца).
Порог боли от давления определяется как сила давления, которая необходима для вызывания субъективно неприятного/болезненного ощущения. Использовался ручной альгометр (Commander Algometer™, JTech). В каждой точке выполнялось два последовательных измерения с интервалом в 20 секунд. Для анализа использовалось среднее значение.
СА также измерялась при помощи уколов механическим стимулято ром (Neuropen®, Owen Mumford) с нанесением силы укола в 40 г в тех же точках. Выраженность боли или неприятного ощущения измеря лась по 100-бальной шкале.
Феномен wind-up (временная суммация боли) исследовался при помощи нанесения серии из 10 уколов на участок кожи площадью 1 см2 на лбу, виске и шее стимулятором Neuropen®. Участники исследования оценивали силу единичного укола и всей серии.
Мигательный рефлекс (МР) вызывался при помощи электрической стимуляции правого надглазничного нерва, подаваемой через поверхностные электроды диаметром 5 мм. Катод располагался над наглазничным отверстием, а анод приблизительно на 2 см выше на коже лба. Наносились одиночные электрические стимулы прямоугольной формы длительностью 0,2 мс с произвольными интервалами не менее 30 секунд для минимизации габитуации и регистрировались четкие R1-, R2- и R3-компоненты мигательного рефлекса. В работе анализировались пороги возникновения позднего компонента R3, для которого описан полисинаптический путь, проходящий от ствола головного мозга до спинального ядра тройничного нерва и затем в латеральную ретикулярную формацию.
Ноцицептивный флексорный рефлекс (НФР) регистрировался при стимуляции правого икроножного нерва трендами длительностью 20 мс и частотой 300 Гц с произвольными интервалами не менее 15 секунд. Катод располагался в проекции нерва, а анод на 2 см ниже в области латеральной лодыжки. Референтный электрод располагался над сухожилием двуглавой мышцы бедра, а заземляющий — на середине голени. Регистрировался порог возникновения R3-ответа и порог субъективной болевой чувствительности (когда пациент болевое ощущение оценивал на 5 баллов по 10-бальной шкале ВАШ). Также рассчитывалось соотношение порог боли/порог рефлекса. R3-компонент замыкается через ретикулярную формацию ствола мозга.
Результаты анализировались при помощи компьютерного пакета Statistica (U-тест Манна–Уитни для сравнения групп, корреляционный тест Спирмена, точный тест Фишера для сравнения пропорций, например, распространенности аллодинии). Все показатели приведены в формате Х ± SD.
Результаты исследования
1. Клинические и демографические характеристики пациентов
Группа ХЕГБ была представлена 28 пациентами с ХМ, 31 пациентом с ХГБН и 10 пациентами со смешанными формами ГБ (ХМ или ХГБН в сочетании с цервикогенной ГБ) в соответствии с критериями ICHD-2. В группу вошли 57 женщин и 12 мужчин, средний возраст 40 лет. Средняя частота ГБ составила 25 дн./мес, сила боли 7 баллов. При общей длительности ГБ в анамнезе в 19 лет, наши пациенты страдали ХЕГБ в среднем 6 лет. О злоупотреблении анальгетическими препаратами сообщили 33% пациентов (табл. 1).
Таблица 1
Клинические и демографические характеристики пациентов и контроля
| ХЕГБ | ЭМ | Контроль | |
| Число пациентов | 69 | 30 | 15 |
| Пол, ж:м | 57:12 | 28:2 | 10:5 |
| Возраст, лет | 40,1 ± 12,3 | 37,3 ± 10,5 | 43,1 ± 18,1 |
| Частота ГБ, дн./мес | 25,2 ± 6,0 | 4,7 ± 1,3 | |
| Сила боли, ВАШ | 7,1 ± 1,9 | 7,7 ± 1,2 | |
| Длительность ГБ, лет | 18,2 ± 12,7 | 16,3 ± 9,7 | |
| Длительность ХЕГБ, лет | 5,7 ± 7,0 | – | |
| ХМ:ХГБН:Смеш. | 28:31:10 | – | |
| Абузус | 20 (33%) | 1 | |
| Кожная аллодиния (анкета) | 79% | 46% | |
| Сила боли во время исследования, ВАШ | 2,3 ± 1,9 |
По данным анкеты аллодинии, в группе ХЕГБ распространенность ЦС во время интенсивной ГБ составила 79%.
2. Статическая аллодиния, феномен wind-up и порог R3 МР и НФР у пациентов с ХЕГБ
Чувствительность к боли от давления достоверно выше в группе ХЕГБ во всех точках, кроме висков, к боли от укола и wind-up во всех точках, кроме лба, по сравнению с группой контроля.
Для удобства расчетов использовался индекс альгометрии. Это сумма порогов боли от давления во всех точках. Так как нет данных о том, какой порог боли от давления указывает на аллодинию, мы использовали группу контроля для получения нормативных данных. Об аллодинии свидетельствует индекс, выше которого указали свои пороги 95% участников группы контроля (в нашем исследовании пороговый индекс альгометрии составил 41,9 фунта). Таким образом, распространенность ЦС во время наименьшей боли в группе ХЕГБ составила 70%. Группа ХЕГБ достоверно отличалась от контроля по индексу альгометрии.
Более того, отсутствие различий в болевых порогах справа и слева, независимо от преимущественной стороны боли при ее усилениях, говорит о стабильности ЦС, так как в приступе мигрени аллодиния всегда развивается на стороне боли и переходит на противоположную сторону, шею и плечи только при длительных приступах.
Для определения нормативных данных порога R3 МР это исследование было проведено на 15 участниках группы контроля. По нашим данным, порог R3-компонента составил 9,6 ± 1,5 мА. В группе ХЕГБ выявлено достоверное снижение порога R3 мигательного рефлекса (7,6 ± 2,16 мА). Нормативный порог НФР составил 10,3 ± 1,7 мА, порог боли 9,8 ± 1,8 мА. В группе ХЕГБ выявлено достоверное снижение порога НФР (9,0 ± 2,2 мА) и порога боли (6,2 ± 1, мА).
3. Статическая аллодиния, феномен wind-up в группе сравнения с ЭМ
Для изучения закономерностей развития ЦС и ее влияния на хронизацию ГБ была исследована группа пациентов с ЭМ с частотой ГБ более 2 дн./мес и менее 15 дн./мес. Возраст пациентов, длительность заболевания и сила боли не отличались в группах ЭМ и ХЕГБ. Средняя частота приступов составила 5,2 дн./мес.
У пациентов группы ЭМ выявлены достоверно более высокие пороги боли от давления и укола во всех точках по сравнению с группой ХЕГБ. Пороги боли при ЭМ достоверно не отличались от показателей контрольной группы испытуемых, что свидетельствует об отсутствии СА при эпизодической мигрени в межприступном периоде. Средний индекс wind-up, напротив, достоверно не различался при ЭМ и ХЕГБ.
Таким образом, группа ЭМ отличается от контроля только по индексу wind-up и от ХЕГБ по остальным показателям сенситизации.
Пациентов с ЭМ можно разделить на 2 подгруппы по индексу wind-up: с высоким и низким индексом. Точка раздела была определена аналогично точке раздела для альгометрии и составила 14,1. В подгруппе с более высоким wind-up выявлена более высокая частота приступов (7,5 дн./мес vs. 3,5 дн./мес) и меньшая длительность заболевания (12,1 года vs. 19,1 года). В подгруппе пациентов, указывающих на признаки кожной аллодинии в анамнезе, выявлена большая частота приступов.
4. Терапия венлафаксином
В качестве профилактического лечения головной боли 18 пациентам из вышеописанной группы пациентов с ХЕГБ был назначен прием венлафаксина (Велафакс®) курсом продолжительностью 1,5 месяца. Схема дозирования: 37,5 мг (18,9 мг × 2 раза в сутки) в течение 7 дней с последующим повышением до 75 мг (37,5 мг × 2 раза в сутки).
5 пациентов (28%) закончили исследование преждевременно: 3 пациента (17%) из-за побочных эффектов, развившихся на стадии титрования препарата и помешавших поднять дозу до минимальной терапевтической; 2 пациента (11%) — из-за отсутствия эффекта от лечения. 13 пациентов прошли полный курс лечения и были включены в анализ. Им также было проведено повторное обследование (аналогичное описанному выше) после окончания 6-недельного курса лечения.
По результатам лечения было достигнуто достоверное снижение средней силы боли (с 6,6 до 4 баллов) и ее частоты (с 26 до 12 дн./мес). У 10 пациентов (77%) частота боли снизилась достоверно, а 54% пациентов отметили как минимум 50%-ное урежение ГБ. У 70% пациентов было достигнуто урежение ГБ более чем на 10 дн./мес (табл. 2).
Таблица 2
Результаты лечения венлафаксином
| До лечения | После лечения | р | |
| Сила боли, ВАШ | 6,6 ± 1,1 | 4,0 ± 2,0 | 0,0005* |
| Частота ГБ | 26,0 ± 4,7 | 12,0 ± 10,7 | 0,0001* |
| Количество анальгетиков | 21,8 ± 22,7 | 5,1 ± 9,3 | 0,005* |
| Индекс альгометрии | 40,6 ± 12,8 | 53,8 ± 13,1 | 0,0003* |
| Индекс боли от укола | 48,2 ± 49,8 | 25,3 ± 42,2 | 0,117 |
| Индекс wind-up | |||
| Аллодиния | 3,7 ± 1,6 | 1,1 ± 1,2 | 0,003* |
| МР R3 | 7,3 ± 1,9 | 9,2 ± 3,0 | 0,023* |
| НФР порог боли | 6,6 ± 4,13 | 7,6 ± 2,6 | 0,100 |
| НФР порог рефлекса | |||
| НФР боль/рефлекс | 0,57 ± 0,2 | 0,8 ± 0,2 | 0,002* |
* достоверные различия.
Заметное снижение частоты и интенсивности ГБ позволило пациентам сократить количество принимаемых анальгетиков (с 21,8 до 5,1 таблетки в месяц), что значительно снижает риск развития абузусной ГБ.
Кроме того, в ходе лечения было достигнуто достоверное повышение индекса альгометрии до нормальных значений и уменьшение выраженности и распространенности аллодинии. У 54% пациентов клинические признаки аллодинии исчезли полностью.
По данным нейрофизиологических исследований, порог R3 МР достоверно повысился и достиг нормального диапазона значений (с 7,3 до 9,2 мА). Пороги боли и рефлекса НФР, а также соотношение порог боли/порог рефлекса также имели тенденцию к повышению, но не достигли нормальных значений.
78% пациентов указали на наличие побочных эффектов в ходе лечения. Наиболее частыми среди них были: тошнота, урежение стула, нарушение концентрации внимания, снижение аппетита. У большинства пациентов эти эффекты были легкими и быстро проходящими. Они развивались в большинстве случаев в течение первой недели приема (на субтерапевтической дозе в 37,5 мг) и исчезали в среднем через 5–7 дней, что не препятствовало повышению дозы до терапевтической.
Обсуждение
В группе пациентов с ХЕГБ выявлена сенситизация центральных ноцицетивных структур — статическая аллодиния, которая сохраняется даже в период наименьшей боли или ее отсутствия. В то же время при ЭМ у большинства пациентов в межприступном периоде аллодиния отсутствует. Однако в группе ЭМ выявляются также пациенты с повышенным индексом wind-up, т. е. те, у кого признаки сенситизации проявляются даже в межприступном периоде. У таких пациентов отмечена более высокая частота приступов и меньшая длительность заболевания. Можно сделать вывод о том, что со временем элементы ЦС не полностью исчезают после окончания мигренозного приступа и пациент становится более восприимчивым к следующему приступу, т. е. встает на путь хронизации ГБ. После того как боль приобретает ежедневный или почти ежедневный характер, она существует самостоятельно, независимо от наличия или отсутствия провоцирующих факторов, и поддерживается в результате центральной сенситизации ноцицептивных структур.
Более низкая длительность ЭМ в подгруппе с высоким wind-up говорит о том, что сам фактор длительности заболевания не приводит к хронизации ГБ. Из клинического опыта известно, что некоторые пациенты могут в течение многих лет страдать ЭМ с неизменной частотой приступов. У другой части пациентов частота приступов начинает неуклонно нарастать вскоре после дебюта заболевания. Таким образом, измерение феномена wind-up позволяет выделить пациентов, у которых началась динамика ЭМ в направлении хронизации и трансформации ГБ.
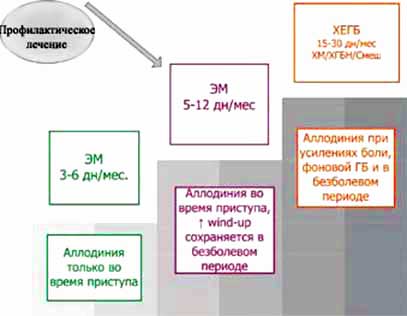
По нашим данным, пациентов с ГБ можно разделить на несколько стадий вне зависимости от диагноза по критериям ICHD-2 (рисунок):
- эпизодическая ГБ с признаками аллодинии только во время приступа;
- эпизодическая ГБ, при которой повышение wind-up сохраняется между приступами;
- ХЕГБ со стабильными признаками ЦС во время усилений боли, фоновой ГБ и безболевом периоде.
Рисунок. Стадии развития ГБ

Выявление ЦС с помощью простого метода wind-up у пациентов с эпизодической ГБ в межприступном периоде позволяет выделить группу риска, уже вступившую на путь хронизации ГБ, и является показанием к началу профилактического лечения.
В ходе исследования было показано, что венлафаксин является эффективным и безопасным средством для урежения ГБ. Профилактическое лечение Велафаксом приводит к выраженному клиническому облегчению состояния пациентов, сокращению приема анальгетиков. Позитивный эффект препарата подтверждается уменьшением выраженности аллодинии, а также нормализацией порога болевого R3-компонента мигательного рефлекса, который отражает функциональное состояние стволовых структур и спинномозгового ядра тройничного нерва, участвующих в поддержании ЦС.
По вопросам литературы обращайтесь в редакцию.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
Велафакс на страже хорошего настроения и душевного спокойствия
Велафакс (Velafax) – медикамент, который применяется в психотерапии и неврологии.
Химически представляет собой антидепрессант, который не относится ни к одной группе известных антидепрессантов (СИОЗС, СИОЗСН, трициклические, тетрациклические).
Является рацематом двух активных энантиомеров.
Компоненты лекарства
Выпускается препарат в таблетках. Они продолговатые, имеют светло-желтый или желтый оттенок. С одной стороны такой таблетки имеется насечка с названием компании – производителя, а с другой находится делительная риска.
В одном блистере 14 таблеток. В упаковке находится два или четыре блистера.
Действующее вещество лекарства – гидрохлорид венлафаксина, концентрация которого в каждой таблетке 42,42 или 84,86 миллиграмм.
Структурная формула гидрохлорид венлафаксина
Также в составе таблеток присутствуют вспомогательные компоненты:
- кукурузный крахмал;
- микрокристаллическая целлюлоза;
- коллоидный диоксид кремния;
- стеарат магния;
- натрия карбоксиметилкрахмал;
- тальк.
Для окраски используется желтый оксид железа.
Фармакологический профиль
Является сильным антидепрессантом. Действующий компонент медикамента и его метаболит ОДВ (О-десметилвенлафаксин) – селективные ингибиторы обратного захвата серотонина и норадреналина. Также незначительно стимулирует синтез допамина.
Активное вещество препарата активизирует передачу нервного импульса в нервную систему.
Всасывается органами пищеварительного тракта. Максимальная концентрация действующего вещества достигается через 2 – 4 часа. При прохождении метаболизируется в печени.
Связь действующих компонентов с плазменными белками составляет до 30%. Выводится преимущественно при мочеиспускании.
Сфера применения и противопоказания
Велафакс назначают при депрессии различной этиологии с признаками тревоги или без таковой, также возможно применение средства в комплексной терапии тревожного расстройства.
Важно знать, что Велафакс не назначают в таких случаях:
- печеночная недостаточность;
- параллельно с приемом ингибиторов МАО;
- патологии почек при клиренсе креатинина меньше 10 мл за минуту;
- период вынашивания ребенка;
- грудное вскармливание;
- детский возраст.
Кроме того, не назначают лекарство при высокой чувствительности к его компонентам.
Необходим врачебный контроль при лечении пациентов, которые страдают гипертензией, учащением сердцебиения, стенокардией, закрытой глаукомой, гиповолемией, гипонатриемией, суицидальным поведением.
С осторожностью используют лекарство при лечении людей, у которых отмечаются частые судороги, повышается внутриглазное давление, имеется эпилепсия и маниакальное расстройство в анамнезе.
Дозировка и схема лечения
Изначально Велафакс назначают в дозировке по 37,5 миллиграмм дважды в сутки. Через некоторое время дозировку могут увеличивать.
При тяжелой депрессии пьют по одной таблетке два раза в день. Специалисты рекомендуют принимать Велафакс во время употребления еды, запивая водой. Разжевывать таблетки не советуют.
Максимальная доза лекарства в сутки становит не более 375 миллиграмм. При достижении терапевтического эффекта дозировку можно снижать. Чтобы отменить употребление таблеток дозировку необходимо снижать постепенно.
Лечение может длиться до полугода.
Случаи передозировки
Зафиксировано незначительное число случаев передозировки. В таком случае возможны следующие реакции:
- тахикардия (желудочковая или синусовая);
- блокада ножки пучка Гиса;
- гипотензия;
- удлиненный интервал QT;
- брадикардия;
- помутнение или потеря сознания;
- судорожные припадки.
Когда такие симптомы ярко выражены, возможен смертельный исход. Поэтому важной в таком случае является симптоматическая терапия, которая осуществляется под контролем электрокардиографии. Нельзя при передозировке вызывать рвоту. Необходимо вызывать скорую помощь.
Побочные эффекты
Побочные реакции возникают только в случае увеличения дозировки, при соблюдении рекомендуемых терапевтических доз организм хорошо переносит Велафакс.
К побочных реакциям относятся различные нарушения со стороны следующих систем:
- сердечно-сосудистая – гипотензия (постуральная или артериальная), учащение пульса;
- пищеварительная – тошнота, сухость в ротовой полости, запоры, рвота, потеря аппетита;
- мочеполовая – задержка мочеиспускания, меноррагия, нарушение эрекции или эякуляции;
- нервная – расстройства сна, головокружения, тремор конечностей, повышенный тонус мышц, апатия, серотониновый синдром, галлюцинации, головная боль, мышечные спазмы;
- кроветворная – тромбоцитопения, экхимоз.
Кроме того, часто возникают аллергические реакции, которые проявляются в виде высыпаний на кожных покровах или анафилактического шока. Также возможна перманентная усталость и общая слабость.
Среди побочных эффектов наблюдаются изменения параметров печеночных проб, повышение значений холестерина в крови, потеря веса, гипонатриемия, нарушение зрения.
Если такие реакции наблюдаются, то необходимо сообщить об этом врачу. В таком случае он выпишет аналог или уменьшит дозировку лекарства.
Особые пациенты и указания
Больным преклонного возраста препарат назначается в минимальной дозировке. Если необходимо увеличение дозировки, то пациент должен находиться под постоянным врачебным контролем.
Беременность является прямым противопоказанием к применению Велафакса. Активные компоненты могут проникать в грудное молоко, поэтому лекарство не разрешается назначать при лактации. Детям, не достигшим 18-летнего возраста, лекарство также употреблять нельзя.
При заболеваниях почек легкой тяжести дозировка не требует коррекции. При среднем поражении почек суточную дозу необходимо снижать. Тяжелые патологии являются противопоказанием для приема лекарства.
При легкой и средней степени нарушения печени дозировку необходимо корректировать. Если у пациента печеночная недостаточность тяжелой формы, то таблетки употреблять не разрешается.
При употреблении лекарства важно учитывать, что оно имеет эффект отмены. В случае резкого отказа от приема медикамента возможно возникновение бессонницы, анорексии, головной боли, раздражительности, парестезии, тревожности. Именно поэтому дозировку необходимо понижать постепенно.
Важно следить за артериальным давлением при употреблении таблеток, поскольку в некоторых случаях наблюдается его повышение.
Алкогольные напитки не разрешается принимать пациентам, которые лечатся Велафаксом.
Взаимодействие с другими лекарствами
С другими препаратами Велафакс имеет такое лечебное взаимодействие:
- одновременный прием с ингибиторами МАО запрещен, назначается только через 14 суток после окончания лечебного курса;
- при приеме Диазепама и Имипрамина не наблюдается изменений метаболитов и фармакокинетики;
- нельзя принимать Клозапин, иначе развиваются побочные действия;
- при назначении Галоперидола наблюдается усиление терапевтического эффекта обоих медикаментов;
- Циметидин угнетает метаболизм активного вещества Велафакса.
Из практики: мнение врачей и советы пациентов
Отзывы специалистов и мнение пациентов, которые пропивали Велафакс курсами.
Велафакс является очень сильным антидепрессантом. Сразу скажу, что подходит препарат не всем. Пациенты, которые принимали таблетки, сразу же чувствовали себя лучше – их состояние быстро стабилизировалось.
Побочные явления обычно наблюдались на начальных стадиях лечения. Наиболее часто среди них – снижение аппетита и тошнота.
Олег Станиславович, психотерапевт
Когда начала принимать этот препарат, сразу же начались побочные явления – болела голова, тошнило, аппетит снизился. Позже эти явления прекратились, но я столкнулась с новой проблемой – очень трудно отменить его употребление.
Также я читала, что были и смертельные исходы при приеме этих таблеток. Поэтому не советую их пробовать. К тому же и цена на них недешевая.
Ольга, 49 лет
Пил лекарство от депрессии полгода. Состояние заметно улучшилось – захотелось жить дальше и радоваться. Эффекта отмены, которым часто пугают, не заметил. Просто важно снижать дозы строго по предписанию специалиста.
Константин, 52 года
Что будет, если принимать Венлафаксин в течении 10 лет:
Пациенты рекомендуют принимать данные таблетки исключительно по назначению специалиста, придерживаясь всех дозировок и схемы лечения.
Основным преимуществом лекарства является его эффективность при депрессивных расстройствах. Минусами считаются большой перечень побочных явлений, эффект отмены и опасные состояния при передозировке.
Покупка и хранение
Велафакс можно купить в аптеке по цене от 550 рублей при дозировке 37,5, и от 690 рублей при дозировке 75 мг.
Данное медикаментозное средство можно хранить до двух лет при рекомендованных условиях. Для хранения необходима температура до 25 градусов. Находиться медикамент должен в труднодоступном для детей месте, в которое не попадают солнечные лучи.
Средство отпускается в фармацевтических учреждениях исключительно по врачебному рецепту.
Чем можно заменить?
По действующему веществу аналогами Велафакса являются:
Использованные источники: neurodoc.ru
ПОХОЖИЕ СТАТЬИ:
Головокружение без головной боли и тошноты у женщин
Симптомы температура 37 слабость головная боль насморк
Головная боль сжимающая как обруч
Пучковые головные боли диагностика
Нестандартные способы лечения головной боли
Головная боль перенапряжения лечение
Венлафаксин и лечение хронической боли
Ноцицептивная передача импульса предполагает вовлечение восходящих афферентных соматосенсорных, спиноталамических путей, которые проходят через пластину дорсального рога спинного мозга. Эти ноцицептивные импульсы модулируются на уровне пластины заднего рога через активацию нисходящих тормозных путей, происходящих из околоводопроводного серого вещества мозга. И серотонин, и норадреналин вовлекаются в нисходящие тормозные механизмы и способствуют изменениям нейрохимической передачи в спинном мозге. Эти изменения могут облегчать особождение субстанции Р, нейротрансмитера, усиливающего ноцицептивную передачу, а также влияют на эффекты эндогенных эндорфинов. Результаты вышеприведенных исследований поддерживают предположение о том, что анальгетический эффект антидепрессантов является результатом внутренних анальгетических свойств молекул антидепрессантов, а не косвенного влияния антидепрессантов на боль через уменьшение депрессии или общий седативный эффект (Ansari A.).
Как было отмечено, Венлафаксин является ингибитором обратного захвата серотонина и норадреналина (Muth E.A., Haskins J.T., 1986; Muth E.A., Moyer J.A., 1991). Посредством этого важного механизма обеспечивается купирование нейропатической боли. Венлафаксин не связывается с мускарин-холинергическими, гистаминовыми и α1-адренергическими рецепторами, благодаря чему при назначении Венлафаксина удается избежать многих нежелательных явлений, которые развивающихся при применении трициклических антидепрессантов.
Клинические исследования указывают на то, что применение Венлафаксина является хорошим методом лечения для пациентов с хроническими болевыми синдромами в рамках большого депрессивного или генерализованного тревожного расстройства. Это важно, поскольку более чем у 40% пациентов с большим депрессивным расстройством имеются хотя бы один болевой симптом (головная боль, боль в спине, боль в суставах, боль в конечностях или боль в желудочно-кишечном тракте) (Ohayon M., 2003). Применение Венлафаксина позволяет снизить и уровень депрессии, и выраженность болевых проявлений.
Венлафаксин-XR назначается при большом депрессивном, генерализованном тревожном и социальном тревожном расстройствах в дозах от 75 до 225 мг/сут (Wyeth Pharmaceuticals, 2003). Для некоторых пациентов эффективными могут быть низкие дозы Венлафаксина. Лечение можно начинать с 37,5 мг/сутки с постепенным увеличением дозы в течение 4-7 дней до 75 мг/сутки.
Проведенные исследования показали, что анальгетический эффект Венлафаксина обусловлен механизмами, не связанными с депрессией. В связи с этим Венлафаксин оказался эффективным и при болевых синдромах, не связанных с депрессией и тревогой.
Хотя показания назначения Венлафаксина при хронической боли еще не включены в инструкцию по применению, имеющиеся данные указывают на то, что при большинстве болевых синдромов эффективной является доза 75-225 мг/сутки. Данные рандомизированных, контролируемых исследований показали, что облегчение боли наступает через 1-2 недели после начала лечения. Тем не менее, некоторым пациентам требуется 6-недельный курс лечения для того чтобы анальгетический эффект Венлафаксина стал очевидным.
Самым частым побочных эффектом Венлафаксина, обнаруженном при лечении боли, является тошнота. Другими побочными эффектами являются ажитация, анорексия, запоры, головокружение, сухость во рту, головная боль, инсомния, сонливость, сексуальные расстройства, рвота.
Венлафаксин продемонстрировал противоболевой эффект на различных моделях животных, на здоровых добровольцах и у пациентов с некоторыми хроническими болевыми синдромами, такими как нейропатическая боль, головная боль (мигрень), фибромиалгия, постмастэктомическая боль. Венлафаксин может стать полезным пополнением в списке антидепрессантов, применяемых для лечения хронической боли. В настоящее время показание Венлафаксина «лечение хронической боли» еще не зарегистрировано. Необходимы дальнейшие исследования для уточнения эффективности, способов дозирования и безопасности Венлафаксина при различных болевых синдромах.
Использованные источники: velafax.paininfo.ru
ПОХОЖИЕ СТАТЬИ:
Головные боли боль в желудке горечь во рту
Какие камни помогают при головной боли
У ребенка головные боли и боль в ногах руках
Заложен нос головная боль 37
Народные лекарства от головного боли
Какие лекарства от головной боли можно при лактации
Венлафаксин при головной боли
Было проведено несколько исследований по оценке эффективности Венлафаксина в профилактике и лечении головной боли (Adelman L.C., et al., 2000; Kathpal G.S., 1998; Nascimento E.D., 1998; Diamond S., 1995; Dwight M.M. et al., 1998; Reuben S. et al., 2002).
Сто пятьдесят пациентов с мигренью с аурой и без ауры (длительность заболевания от 1 до 4 лет) приняли участие в проспективном, плацебо-конролируемом, двойном слепом исследовании, в котором сравнивалась эффективность Венлафаксина, флуоксетина, сертралина и пароксетина при профилактическом лечении мигрени (Kathpal GS., 1998). Лечение продолжалось 3 месяца и более. Больше пациентов, принимавших Венлафаксин (доза неизвестна), отметили улучшение в своем состоянии по сравнению с плацебо и другими препаратами, с которыми проводилось сравнение. Двое пациентов из группы Венлафаксина досрочно прекратили лечение из-за неспецифических побочных эффектов.
В центре головной боли (Adelman LC., 2000) был проведен ретроспективный анализ данных 97 пациентов с хронической головной болью (хроническая головная боль напряжения, мигрень с аурой и без ауры, сочетание мигрени и головной боли напряжения) со стажем заболевания не менее 2 лет, получавших лечение венлафаксином в дозе 75 мг 2 раза в день. Тридцать семь процентов включенных в анализ пациентов отметили снижение количества приступов, 45% не обнаружили никаких изменений, а у 18% пациентов увеличилось количество головных болей.
Ретроспективное открытое исследование по изучению влияния Венлафаксина-XR при лечении мигрени и хронической головной боли напряжения показало достоверное снижение количества головных болей в месяц на последнем визите по сравнению с началом лечения в обеих группах. В группе мигрени среднее количество приступов головной боли в месяц снизилось с 16,1 до 11,1. В группе головной боли напряжения среднее количество эпизодов головной боли снизилось с 24 до 15,2 (Adelman L.C. et al., 2001).
Н.В. Латышева и Е.Г. Филатова (2008) исследовали влияние Венлафаксина (препарат компании «Плива» Велафакс ® ) при хронической ежедневной головной боли. В исследовании приняли участие 69 пациентов с хронической ежедневной головной болью и 30 пациентов с эпизодической мигренью, а также 15 участников группы контроля. Целью работы явилось изучение феномена центральной сенситизации при хронической эпизодической головной боли, ее роли в хронификации головной боли и эффективности Венлафаксина для ее урежения.
В ходе исследования было показано, что Венлафаксин является эффективным и безопасным средством для урежения ГБ. Профилактическое лечение Велафаксом приводит к выраженному клиническому облегчению состояния пациентов, сокращению приема анальгетиков. По мнению авторов, позитивный эффект препарата может быть связан с уменьшением выраженности аллодинии, что было подтверждено нормализацией порога болевого R3-компонента мигательного рефлекса, который отражает функциональное состояние стволовых структур и спинномозгового яд?


