Роль структур головного мозга в формировании боли
Полноценное чувственное восприятие боли организмом без участия коры головного мозга невозможно. Ретикулярная формация ствола (РФ) передает болевую информацию в неспецефические ядра таламуса, затем в кору, а также в гипоталамус и лимбическую систему, усиливает и пролонгирует защитные реакции спинного мозга и ствола, вовлекает в ответ вегетативную (особенно симпатическую) нервную систему. Повышение активирующего влияния восходящей РФ вызывает реакции возбуждения, настораживания.
Первичное проекционное поле болевого анализатора находится в соматосенсорной коре задней центральной извилины. Оно обеспечивает восприятие «быстрой» боли и идентификацию места ее возникновения на теле. Для более точной идентификации локализации боли в процесс обязательно включается и нейроны моторной коры передней центральной извилины.
Вторичное проекционное поле расположено в соматосенсорной коре на границе пересечения центральной борозды с верхним краем височной доли. Нейроны данного поля имеют двусторонние связи с ядрами таламуса, что позволяет этому полю избирательно фильтровать, проходящие через таламус возбуждения болевого характера. А это в свою очередь позволяет данному полю вовлекаться в процессы, связанные с извлечением из памяти энграммы необходимого поведенческого акта, его реализации в деятельности эффекторов и оценки качества достигнутого полезного результата. Двигательные компоненты болевого поведения формируются в совместной деятельности моторной и премоторной коры, базальных ганглиев и мозжечка.
Таламус учавствует в передаче и переработке болевой информации: специфические ядра таламуса обеспечивают анализации болевого раздражения, его силы и длительности, неспецифические ядра таламуса учавствуют в формировании мотивационно-аффективного аспекта боли.
Лобная кора играет важную роль в восприятии боли. Она обеспечивает самооценку боли (ее когнитивный компонент) и формирование целенаправленного болевого поведения.
Лимбическая система (поясная извилина, гиппокамп, зубчатая извилина, миндалевидный комплекс височной доли) получает болевую информацию от передних ядер таламуса и формирует эмоциональный компонент боли, запускает вегетативные, соматические и поведенческие реакции, обеспечивающие приспособительные реакции к болевому раздражителю.
Статьи и публикации:
Акселерация. Медицинские и педагогические проблемы
акселерации. Особенности акселерации в условиях Кольского Заполярья
Акселерация – это ускорение роста и развития детей и подростков по сравнению с предшествующими поколениями. Явление акселерации наблюдается прежде всего в экономически развитых странах.
Термин «акселерация» был введен в научный обиход Е. …
Онтогенез растений
Поскольку растения чрезвычайно разнообразны, то для них характерны специфические онтогенезы. Можно сказать, что содержание онтогенеза растений зависит от их таксономической принадлежности.
В случае одноклеточных организмов растительной п …
Синтез сложных эфиров, катализируемый липазами
Синтез сложных эфиров монофункциональных спиртов, катализируемый липазами, с хорошими выходами протекает в микроэмульсиях. Липазы различной природы обладают разной специфичностью по отношению к длине алкильной цепи кислоты и к типу спирта …
Источник
3.1 Участие ретикулярной формаци в проведении боли
Роль
ретикулярной формации в проведении
боли была установлена последованиями
Г. Мэгуна. Влияние беловых раздражений
связано с функцией ретикулярной формации,
особенно с её восходящей системой.
Она
не только является важной релейной
(второй) станцией передачи ноцицептивной
информации, но и осуществляет ее анализ
и интеграцию. Здесь оканчиваются пути
и (или) коллатерали восходящих систем
и начинается диффузная проприоретикулярная
система, а также восходящие проекции к
вентробазальным и интраламинарным
ядрам таламуса и далее — в соматосенсорную
зону коры головного мозга. Через связи
ретикулярной формации с гипоталамусом,
базальными ядрами и лимбическим мозгом
реализуются нейроэндокринные и
эмоционально-аффективные компоненты
боли, сопровождающие реакции защиты,
бегства или нападения в ответ на
повреждающие воздействия.
Прямые
и опосредованные многочисленные проекции
ретикулярной формации в кору определяют
ее участие в реакциях пробуждения,
настораживания на повреждающие стимулы,
в формировании ощущения боли и ее
психофизиологической оценки.
П.
К.Анохин считал: «Боль представляет
собой совершенно реальное
субъективное
ощущение, что и является её наиболее
характерной чертой».
Боль следует
понимать, как явление физиологическое,
а не анатомическое.
Действительно,
можно привести примеры, когда в организме
нет анатомических изменений, между тем
возникают нередко очень сильные боли,
стресс.
В
клинической практике применяется термин
каузальгия ( жгучая боль), который
используется для характеристики
типичного клинического синдрома,
возникающего при травматических
повреждениях нервов. Особенно богатых
симпатическими волокнами. У человека
обычно возникают ещё так называемые
фантомные болезни после ампутации
органов, т. е. «боль в несуществующем
органе». Такие боли наблюдаются у
животных. Этот факт указывает на то, что
после ампутации, например, пальцев или
конечностей остаётся нередко пожизненно
болевая реакция. Ёё ощущение несомненно,
связанно с появлением постоянных
раздражений определенных зон головного
мозга, в особенности зрительных бугров.
На основании исследований биопотенциалов
головного мозга при болевых (ноцицептивных)
раздражениях установлено, что в восприятии
и проведении болевых ощюшений существенная
роль принадлежит ретикулярной формации
стволовой части мозга. (П. А. Анохин,
1956-1963, В. Г. Агафонов, 1956; B. C. Шевелева,
I960, и др.). Указанные наблюдения позволили
сделать вывод о двух путях передачи
тонизирующих влияний ретикулярной
формации, включающий задний гипоталамус,
— восходящем и нисходящем. По этим же
путям поступают в кору головного мозга
афферентные импульсы. Считают, что при
болевых раздражениях афферентные
импульсы идут по классическому проводящему
пути и посредством коллатеральных
связей опять же поступают в ретикулярную
формацию ствола мозга. В свею очередь,
возбуждение в ретикулярной формации
передаётся коре головного мозга, а в
дальнейшем болевые (ноцицепривные)
раздражения блокируются на уровне
подкорковых аппаратов. Очевидно, боль
как интегральное состояние организма
обуславливается системой сложных
соотношений нервных процессов, именно
на уровне подкорковых аппаратов, так
как здесь происходит расшифровка
(декодирование) поступающих о периферии
афферентных импульсов ( П. А. Анохин ).
Источник
Болевая, или ноцицептивная чувствительность – это восприятие стимулов, вызывающих в организме ощущение боли.
В настоящее время нет общепринятого понятия боли. В узком смысле боль – это неприятное ощущение, возникающее при действии сверхсильных раздражителей, вызывающих структурно-функциональные изменения в организме.
Физиологическая роль боли заключается в следующем:
- Выполняет роль сигнала об угрозе или повреждении тканей организма и предупреждает их.
- Является фактором мобилизации защитно-приспособительных реакций при повреждении его органов и тканей
- Имеет познавательную функцию: через боль человек начиная с раннего детства учится избегать возможные опасности внешней среды.
- Эмоциональный компонент боли выполняет функцию подкрепления при образовании условных рефлексов даже при однократном сочетании условного и безусловного раздражителей.
Причины боли. Боль возникает при нарушении, во-первых, целостности защитных покровных оболочек тела (кожи, слизистых оболочек) и внутренних полостей организма (мозговых оболочек, плевры, брюшины и др.) и, во-вторых, кислородного режима органов и тканей до уровня, вызывающего структурно-функциональные повреждения.
Классификация боли. Выделяют два вида боли:
- Соматическую, возникающую при повреждении кожи и опорно-двигательного аппарата. Соматическую боль подразделяют на поверхностную и глубокую. Поверхностной болью называется боль кожного происхождения, а если ее источник локализован в мышцах, костях и суставах, она называется глубокой болью. Поверхностная боль проявляется в покалывании, пощипывании. Глубокая боль, как правило, тупая, плохо локализуется, обладает тенденцией иррадиировать в окружающие структуры, сопровождается неприятными ощущениями, тошнотой, сильным потоотделением, падением артериального давления.
- Висцеральную, возникающую при повреждении внутренних органов и имеющую аналогичную картину с глубокой болью.
Проекционные и отраженные боли. Существуют особые виды боли – проекционная и отраженная.
В качестве примера проекционной боли можно привести резкий удар по локтевому нерву. Подобный удар вызывает неприятное, трудно описываемое ощущение, распространяющееся на те участки руки, которые иннервируются этим нервом. Их возникновение основано на законе проекции боли: какая бы часть афферентного пути не раздражалась, боль ощущается в области рецепторов данного сенсорного пути. Одна из распространенных причин проекционных болей – это пережатие спинальных нервов в местах их вхождения в спинной мозг в результате повреждения межпозвонковых хрящевых дисков. Афферентные импульсы в ноцицептивных волокнах при такой патологии вызывают болевые ощущения, которые проецируются в область, связанную с травмируемым спинальным нервом. К проекционным (фантомным) болям относятся также боли, которые ощущают больные в области удаленной части конечности.
Отраженными болями называются болевые ощущения не во внутренних органах, от которых поступают болевые сигналы, а в определенных частях кожной поверхности (зоны Захарьина-Геда). Так, при стенокардии кроме болей в области сердца ощущается боль в левой руке и лопатке. Отраженная боль отличается от проекционной боли тем, что она вызывается не прямой стимуляцией нервных волокон, а раздражением каких-либо рецептивных окончаний. Возникновение этих болей связано с тем, нейроны, проводящие болевые импульсы от рецепторов пораженного органа и рецепторов соответствующего участка кожи, конвергируют на одном и том же нейроне спиноталамического пути. Раздражение этого нейрона с рецепторов пораженного органа в соответствии с законом проекции боли приводит к тому, что боль ощущается и в области кожных рецепторов.
Противоболевая (антиноцицептивная) система. Во второй половине ХХ были получены данные о существовании физиологический системы, ограничивающей проведение и восприятие болевой чувствительности. Важным ее компонентом является «воротный контроль» спинного мозга. Он осуществляется в задних столбах тормозными нейронами, которые путем пресинаптического торможения ограничивают передачу болевых импульсов по спиноталамическому пути.
Ряд структур головного мозга оказывает нисходящее активирующее влияние на тормозные нейроны спинного мозга. К ним относятся центральное серое вещество, ядра шва, голубое пятно, латеральное ретикулярное ядро, паравентрикулярное и преоптическое ядра гипоталамуса. Соматосенсорная область коры объединяет и контролирует деятельность структур противоболевой системы. Нарушение этой функции может вызвать нестерпимую боль.
Важнейшую роль в механизмах противоболевой функции ЦНС играет эндогенная опиантная система (опиантные рецепторы и эндогенные стимуляторы).
Эндогенными стимуляторами опиантных рецепторов являются энкефалины и эндорфины. Некоторые гормоны, например, кортиколиберин могут стимулировать их образование. Эндорфины действуют преимущественно через морфинные рецепторы, которых особенно много в головном мозге: в центральном сером веществе, ядрах шва, среднем таламусе. Энкефалины действуют через рецепторы, расположенные преимущественно в спинном мозге.
Теории боли. Существует три теории боли:
- Теория интенсивности. Согласно этой теории боль не является специфическим чувством и не имеет своих специальных рецепторов, а возникает при действии сверхсильных раздражителей на рецепторы пяти органов чувств. В формировании боли участвуют конвергенция и суммация импульсов в спинном и головном мозге.
- Теория специфичности. В соответствии с данной теорией боль является специфическим (шестым) чувством, имеющим собственный рецепторный аппарат, афферентные пути и структуры головного мозга, перерабатывающие болевую информацию.
- Современная теория боли базируется преимущественно на теории специфичности. Было доказано существование специфичных болевых рецепторов.
Вместе с тем в современной теории боли использовано положение о роли центральной суммации и конвергенции в механизмах боли. Наиболее важным достижением в разработке современной теории боли является исследование механизмов центрального восприятия боли и противоболевой системы организма.
Болевые рецепторы (ноцирецепторы)
Болевые рецепторы являются свободными окончаниями чувствительных миелиновых и безмиелиновых нервных волокон, расположенных в коже, слизистых оболочках, надкостнице, зубах, мышцах, органах грудной и брюшной полости и других органах и тканях. Число ноцирецепторов в коже человека примерно 100-200 на 1 кв. см. кожной поверхности. Общее число таких рецепторов достигает 2-4 млн. Выделяют следующие основные виды болевых рецепторов:
- Механоноцицепторы: реагируют на сильные механические раздражители, проводят быструю боль и быстро адаптируются.
- Механотермические ноцицепторы: реагируют на сильные механические и тепловые (более 40 градусов) раздражители, проводят быструю механическую и термическую боль, быстро адаптируются.
- Полимодальные ноцицепторы: реагируют на механические, термические и химические раздражители, проводят плохо локализованную боль, медленно адаптируются.
Проводящие пути болевой чувствительности. Болевая чувствительность туловища и конечностей, внутренних органов, от рецепторов которых отходят волокна первых нейронов, находятся в спинальных узлах. Аксоны этих нейронов входят в спинной мозг и переключаются на вторые нейроны, расположенные в задних рогах. Часть болевой импульсации первых нейронов переключается на мотонейроны сгибателей и участвует в формировании защитных болевых рефлексов. Основная часть болевой импульсации (после переключения в задних рогах) поступает в восходящие пути, среди которых главными являются боковой спиноталамический и спинно-ретикулярный.
Болевая чувствительность лица и полости рта передается по волокнам первых нейронов тройничного ганглия, которые переключаются на вторые нейроны, расположенные преимущественно в спинальном ядре (от рецепторов кожи) и мостовом ядре (от рецепторов мышц, суставов) тройничного нерва. От этих ядер болевая импульсация проводится по бульботаламическим путям. По этим путям проводится и часть болевой чувствительности от внутренних органов по афферентным волокнам блуждающего и языкоглоточного нервов в ядро одиночного пути.
Таким образом, болевые ощущения передаются в мозг с помощью двух систем – медиальной и латеральной.
Медиальная система проходит через центральные участки мозга. Она ответственна за стойкую боль, передает сигналы в лимбическую систему, участвующую в эмоциональном поведении. Именно эта медиальная система обеспечивает эмоциональный компонент боли, который выражается в таких ее характеристиках, как «ужасная», «невыносимая» и т.п. Медиальная система состоит преимущественно из мелких волокон и завершается в таламусе. Эта система проводит сигналы медленно, не приспособлена для точного и быстрого проведения информации о сильных раздражителях в критических ситуациях. Она передает диффузные неприятные ощущения.
Латеральная система боли состоит из нервных трактов, проецирующихся в соматосенсорную кору головного мозга. Она наиболее активна при внезапной, резкой (фазической) боли, боли с четко выраженной локализацией. Латеральные пути отвечают за сенсорное качество боли, т.е. характер ощущения – пульсирующая боль, укол, жжение и т.д. Активность латеральной системы быстр затухает, поэтому фазическая боль кратковременна, она подвергается мощному торможению со стороны других структур.
Роль структур головного мозга в формировании боли
Ретикулярная формация ствола передает болевую информацию в неспецифические ядра таламуса, затем в кору головного мозга, а также в гипоталамус и лимбическую систему, усиливает и пролонгирует защитные реакции спинного мозга и ствола, вовлекает в ответ вегетативную (особенно симпатическую) нервную систему.
Таламус участвует в передаче и переработке информации: специфические ядра таламуса обеспечивают анализ локализации болевого раздражения, его силы и длительности, неспецифические ядра таламуса участвуют в формировании мотивационно-аффективного аспекта боли.
Лимбическая система получает болевую информацию от передних ядер таламуса и формирует эмоциональный компонент боли, запускает вегетативные, соматические и поведенческие реакции, обеспечивающие приспособительные реакции к болевому раздражителю.
Кора постцентральной извилины получает болевую информацию в основном от специфических ядер таламуса и создает ощущение боли.
Двигательная кора (совместно с базальными ганглиями и мозжечком) формирует моторные программы болевого поведения.
Лобная кора обеспечивает самооценку боли (ее когнитивный компонент) и формирование целенаправленного болевого поведения. (Перерезка связей между лобной корой и таламусом – лоботомия- сохраняет ощущение боли у больных, но она их не беспокоит).
Источник
Физиология
боли
В
узком смысле слова боль – это неприятное
ощущение, возникающее при действии
сверхсильных раздражителей, вызывающих
структурно-функциональные нарушения
в организме. Отличия боли от других
ощущений в том, что она не информирует
мозг о качестве раздражителя, а указывает
на то, что раздражитель является
повреждающим. Другой особенностью
болевой сенсорной системы является
наиболее сложной и мощный ее эфферентный
контроль.
Болевой
анализатор запускает в ЦНС несколько
программ ответа организма на боль.
Следовательно, боль имеет несколько
компонентов. Сенсорный компонент
боли характеризует ее как неприятное,
тягостное ощущение; аффективный компонент
– как сильную отрицательную эмоцию;
мотивационный компонент – как
отрицательную биологическую потребность,
запускающую поведение организма,
направленное на выздоровление. Моторный
компонент боли представлен различными
двигательными реакциями: от безусловных
сгибательных рефлексов до двигательных
программ антиболевого поведения.
Вегетативный компонент характеризует
нарушение функций внутренних органов
и обмена веществ при хронических болях.
Когнитивный компонент связан с самооценкой
боли, боль при этом выступает как
страдание. При деятельности других
систем эти компоненты слабо выражены.
Биологическая
роль боли определяется несколькими
факторами. Боль исполняет роль сигнала
об угрозе или повреждении тканей
организма и предупреждает их. Боль имеет
познавательную функцию: человек через
боль учится избегать возможных опасностей
внешней среды. Эмоциональный компонент
боли выполняет функцию подкрепления
при образовании условных рефлексов.
Боль является фактором мобилизации
защитно-приспособительных реакций
организма при повреждении его тканей
и органов.
Выделяют
два вида боли – соматическую и
висцеральную. Соматическую боль
подразделяют на поверхностную и глубокую
Поверхностная боль может быть ранняя
(быстрая, эпикрическая) и поздняя
(медленная, протопатическая).
Существуют
три теории боли.
1.
Теория интенсивности была предложена
Э.Дарвином и А.Гольдштейнером. По этой
теории боль не является специфическим
чувством и не имеет своих специальных
рецепторов. Она возникает при действии
сверхсильных раздражителей на рецепторы
пяти известных органов чувств. В
формировании боли участвуют конвергенция
и суммация импульсов в спинном и головном
мозге.
2.
Теория специфичности была сформулирована
немецким физиологом М.Фреем. В соответствии
с этой теорией боль является специфическим
чувством, имеющим собственный рецепторный
аппарат, афферентные волокна и структуры
головного мозга, перерабатывающие
болевую информацию. Эта теория в
дальнейшем получила более полное
экспериментальное и клиническое
подтверждение.
3.
Современная теория боли базируется
преимущественно на теории специфичности.
Было доказано существование специфичных
болевых рецепторов. Вместе с тем в
современной теории боли использовано
положение о роли центральной суммации
и конвергенции в механизмах боли.
Наиболее крупными достижениями
современной теории боли является
разработка механизмов центрального
восприятия боли и запуска противоболевой
системы организма.
Болевые
рецепторы
Болевые
рецепторы являются свободными окончаниями
чувствительных миелиновых нервных
волокон Аδ и немиелиновых волокон
С. Они найдены в коже, слизистых оболочках,
надкостнице, зубах, мышцах, суставах,
внутренних органах и их оболочках,
сосудах. Их нет в нервной ткани головного
и спинного мозга. Наибольшая их плотность
имеется на границе дентина и эмали зуба.
Выделяют
следующие основные типы болевых
рецепторов:
1.
Механоноцицепторы и механотермические
ноцицепторы Аδ-волокон реагируют на
сильные механические и термические
раздражители, проводят быструю
механическую и термическую боль, быстро
адаптируются; расположены преимущественно
в коже, мышцах, суставах, надкостнице;
их афферентные нейроны имеют малые
рецептивные поля.
2.
Полисенсорные ноцицепторы С-волокон
реагируют на механические, термические
и химические раздражители, проводят
позднюю плохо локализованную боль,
медленно адаптируются; их афферентные
нейроны имеют большие рецептивные поля.
Болевые
рецепторы возбуждаются тремя видами
раздражителей:
1.
Механические раздражители, создающие
давление более 40г/мм2 при
сдавливании, растяжении, сгибании,
скручивании.
2.
Термические раздражители могут быть
тепловыми (> 450С)
и холодовыми (< 150С).
3.
Химические раздражители, освобождающиеся
из поврежденных клеток тканей, тучных
клеток, тромбоцитов (К+,
Н+,
серотонин, ацетилхолин, гистамин), плазмы
крови (брадикинин, каллидин) и окончаний
ноцицептивных нейронов (вещество Р).
Одни из них возбуждают ноцицепторы (К+,
серотонин, гистамин, брадикинин, АДФ),
другие сенсибилизируют их.
Свойства
болевых рецепторов: болевые рецепторы
имеют высокий порог возбуждения, что
обеспечивает их ответ только на
чрезвычайные раздражители. Ноцицепторы
С-афферентов плохо адаптируются к
длительно действующим раздражителям.
Возможно повышение чувствительности
болевых рецепторов – снижение порога
их раздражения при многократной или
длительной стимуляции, что называется
гипералгезией. При этом ноцицепторы
способны отвечать на стимулы субпороговой
величины, а также возбуждаться
раздражителями других модальностей.
Проводящие
пути болевой чувствительности
Нейроны,
воспринимающие болевую импульсацию.
От болевых рецепторов туловища, шеи и
конечностей Аδ- и С-волокна первых
чувствительных нейронов (их тела
находятся в спинальных ганглиях) идут
в составе спинномозговых нервов и входят
через задние корешки в спинной мозг,
где разветвляются в задних столбах и
образуют синаптические связи прямо или
через интернейроны со вторыми
чувствительными нейронами, длинные
аксоны которых входят в состав
спиноталамических путей. При этом они
возбуждают два вида нейронов: одни
нейроны активируются только болевыми
стимулами, другие – конвергентные
нейроны – возбуждаются также и неболевыми
стимулами. Вторые нейроны болевой
чувствительности преимущественно
входят в состав боковых спиноталамических
путей, которые и проводят большую часть
болевых импульсов. На уровне спинного
мозга аксоны этих нейронов переходят
на сторону, противоположную раздражению,
в стволе головного мозга они доходят
до таламуса и образуют синапсы на
нейронах его ядер. Часть болевой
импульсации первых афферентных нейронов
переключаются через интернейроны на
мотонейроны мышц-сгибателей и участвуют
в формировании защитных болевых
рефлексов. В боковом спиноталамическом
пути выделяют эволюционно более молодой
неоспиноталамический путь и древний
палеоспиноталамический путь.
Неоспиноталамический
путь проводит болевые сигналы по
Аδ-волокнам преимущественно в специфические
сенсорные (вентральные задние) ядра
таламуса, имеющие хорошую топографическую
проекцию периферии тела. Кроме этого
небольшая часть импульсов поступает в
ретикулярную формацию ствола и далее
в неспецифические ядра таламуса.
Передача возбуждения в синапсах этого
пути осуществляется с помощью
быстродействующего медиатора глутамата.
Из специфических ядер таламуса болевые
сигналы передаются преимущественно в
сенсорную кору больших полушарий. Эти
особенности формируют основную функцию
неоспиноталамического пути – проведение
«быстрой» боли и восприятие ее с высокой
степенью локализации.
Палеоспиноталамический
путь проводит болевые сигналы по
С-волокнам преимущественно в неспецифические
ядра таламуса прямо или после переключения
в нейронах ретикулярной формации ствола
мозга. Передача возбуждения в синапсах
этого пути происходит более медленно.
Медиатором является вещество Р. Из
неспецифических ядер импульсация
поступает в сенсорную и другие отделы
коры больших полушарий. Небольшая часть
импульсации поступает и в специфические
ядра таламуса. В основном волокна этого
пути оканчиваются на нейронах 1)
неспецифических ядер таламуса; 2)
ретикулярной формации; 3) центрального
серого вещества; 4) голубого пятна; 5)
гипоталамуса. Через палеоспиноталамический
путь проводится «поздняя», плохо
локализуемая боль, формируются
аффективно-мотивационные проявления
болевой чувствительности.
Кроме
этого болевая чувствительность частично
проводится по другим восходящим путям:
переднему спиноталамическому, тонкому
и клиновидному путям.
Вышеназванные
пути проводят и другие виды чувствительности:
температурную и тактильную.
Роль
коры больших полушарий в восприятии
боли
Полноценное
чувственное восприятие боли организмом
без участия коры головного мозга
невозможно.
Первичное
проекционное поле болевого анализатора
находится в соматосенсорной коре задней
центральной извилины. Оно обеспечивает
восприятие «быстрой» боли и идентификацию
места ее возникновения на теле. Для
более точной идентификации локализации
боли в процесс обязательно включается
и нейроны моторной коры передней
центральной извилины.
Вторичное
проекционное поле расположено в
соматосенсорной коре на границе
пересечения центральной борозды с
верхним краем височной доли. Нейроны
данного поля имеют двусторонние
связи с ядрами таламуса, что позволяет
этому полю избирательно фильтровать,
проходящие через таламус возбуждения
болевого характера. А это в свою очередь
позволяет данному полю вовлекаться в
процессы, связанные с извлечением из
памяти энграммы необходимого поведенческого
акта, его реализации в деятельности
эффекторов и оценки качества достигнутого
полезного результата. Двигательные
компоненты болевого поведения формируются
в совместной деятельности моторной и
премоторной коры, базальных ганглиев
и мозжечка.
Лобная
кора играет важную роль в восприятии
боли. Она обеспечивает самооценку боли
(ее когнитивный компонент) и формирование
целенаправленного болевого поведения.
Лимбическая
система (поясная извилина, гиппокамп,
зубчатая извилина, миндалевидный
комплекс височной доли) получает болевую
информацию от передних ядер таламуса
и формирует эмоциональный компонент
боли, запускает вегетативные, соматические
и поведенческие реакции, обеспечивающие
приспособительные реакции к болевому
раздражителю.
Некоторые
виды болевых ощущений
Существуют
боли, которые названы проекционными или фантомными.
Их возникновение основано на законе
проекции боли: какая бы часть афферентного
пути не раздражалась, боль ощущается в
области рецепторов данного сенсорного
пути. По современным данным в формировании
данного вида болевого ощущения участвуют
все отделы болевой сенсорной системы.
Существуют
также так называемые отраженные боли:
когда боль ощущается не только в
пораженном органе, но и в соответствующем
дерматоме тела. Участки поверхности
тела соответствующего дерматома, где
возникает ощущение боли, назвали зонами
Захарьина – Геда.
Возникновение отраженных болей связано
с тем, что нейроны, проводящие болевую
импульсацию от рецепторов пораженного
органа и кожи соответствующего дерматома,
конвергируют на одном и том же нейроне
спиноталамического пути. Раздражение
этого нейрона с рецепторов пораженного
органа в соответствии с законом проекции
боли приводит к тому, что боль ощущается
и в области кожных рецепторов.
Антиноцицептивная
система
Антиболевая
система состоит из четырех уровней:
спинального, стволового, гипоталамического
и коркового.
1.
Спинальный уровень антиноцицептовной
системы. Важным ее компонентом
является «воротный контроль» спинного
мозга, концепция которого имеет следующие
основные положения: передача болевых
нервных импульсов с первых нейронов на
нейроны спиноталамических путей
(вторые нейроны) в задних столбах спинного
мозга модулируется спинальным воротным
механизмом – тормозными нейронами,
расположенными в желатинозном веществе
спинного мозга. На этих нейронах
оканчиваются разветвления аксонов
различных сенсорных путей. В свою очередь
нейроны желатинозной субстанции
оказывают пресинаптическое торможение
в местах переключения первых и вторых
нейронов болевых и других сенсорных
путей. Часть нейронов являются
конвергентными: на них образуют синапсы
нейроны не только от болевых, но и от
других рецепторов. Спинальный воротный
контроль регулируется соотношением
импульсов, поступающих по афферентным
волокнам большого диаметра (неболевая
чувствительность) и малого диаметра
(болевая чувствительность). Интенсивный
поток импульсов по волокнам большого
диаметра ограничивает передачу болевых
сигналов на нейроны спиноталамических
путей (закрывает «ворота»). Напротив,
интенсивный поток болевых импульсов
по первому афферентному нейрону,
ингибируя тормозные интернейроны,
облегчает передачу болевых сигналов
на нейроны спиноталамических путей
(открывает «ворота»). Спинальный
воротный механизм находится под
постоянным влиянием нервных импульсов
структур ствола мозга, которые передаются
по нисходящим путям как на нейроны
желатинозной субстанции, так и на нейроны
спиноталамических путей.
2.
Стволой уровень антиноцицептивной
системы. К стволовым структурам
противоболевой системы относятся,
во-первых, центральное серое вещество
и ядра шва, образующие единый функциональный
блок, во-вторых, крупноклеточное и
парагигантоклеточное ядра ретикулярной
формации и голубое пятно. Первый
комплекс блокирует
прохождение болевой импульсации на
уровне релейных нейронов ядер задних
рогов спинного мозга, а также релейных
нейронов сенсорных ядер тройничного
нерва, образующих восходящие пути
болевой чувствительности. Второй
комплекс возбуждает почти всю
антиноцицептивную систему (см.рис.1).
3.
Гипоталамический уровень антиноцицептивной
системы, с одной стороны, функционирует
самостоятельно, а с другой – выступает
как настройка, контролирующая и
регулирующая антиноцицептивные механизмы
стволового уровня за счет связей
гипоталамических нейронов разной
ядерной принадлежности и разной
нейрохимической специфичности. Среди
них идентифицированы нейроны, в окончаниях
аксонов которых выделяются энкефалины,
β-эндорфин, норадреналин, дофамин
см.рис.2).
4.
Корковый уровень антиноцицептивной
системы. Объединяет и контролирует
деятельность антиноцицептивных структур
различного уровня соматосенсорная
область коры больших полушарий. При
этом наиболее важную роль в
активации спинальных
и стволовых структур играет
вторичная сенсорная область. Ее нейроны
образуют наибольшее количество волокон
нисходящего контроля болевой
чувствительности, направляющиеся к
задним рогам спинного мозга и ядрам
ствола головного мозга. Вторичная
сенсорная кора видоизменяет активность
стволового комплекса антиноцицептивной
системы. Кроме этого соматосенсорные
поля коры больших полушарий контролируют
проведение афферентных болевых импульсов
через таламус. Кроме таламуса, кора
большого мозга регламентирует прохождение
болевой импульсации в гипоталамусе,
лимбической системе, ретикулярной
формации, спинном мозге. Ведущая роль
в обеспечении кортико-гипоталамических
влияний отводится нейронам лобной коры.
Медиаторы
антиноцицептивной системы
К
медиаторам противоболевой системы
относят пептиды, которые образуются в
головном мозге, аденогипофизе, мозговом
слое надпочечников, желудочно-кишечном
тракте, плаценте из неактивных
предшественников.. Сейчас к опиатным
медиаторам антиноцицептивной системы
относят: 1) ά-, β-, γ-эндорфины; 2) энкефалины;
3) динорфины. Эти медиаторы действуют
на три вида опиатных рецепторов: μ-, δ-,
κ-рецепторы. Наиболее селективным
стимулятором μ-рецепторов являются
эндорфины, δ-рецепторов – энкефалины,
а κ-рецепторов – динорфины. Плотность
μ- и κ-рецепторов высокая в коре больших
полушарий и в спинном мозгу, средняя –
в стволе головного мозга; плотность
δ-рецепторов средняя в коре больших
полушарий и спинном мозгу, малая – в
стволе мозга. Опиоидные пептиды угнетают
действие веществ, вызывающих боль, на
уровне ноцицепторов, уменьшают
возбудимость и проводимость болевой
импульсации, угнетают вызванную реакцию
нейронов, находящихся в составе цепей,
передающих болевую импульсацию. Эти
пептиды поступают к нейронам болевой
сенсорной системы с кровью и ликвором.
Выделяются опиоидные медиаторы в
синаптических окончаниях нейронов
противоболевой системы. Аналгезирующий
эффект эндорфинов высокий в головном
и спинном мозге, эффект энкефалинов
в этих структурах средний, эффект
динорфинов в головном мозге низкий,
в спинном мозге – высокий.

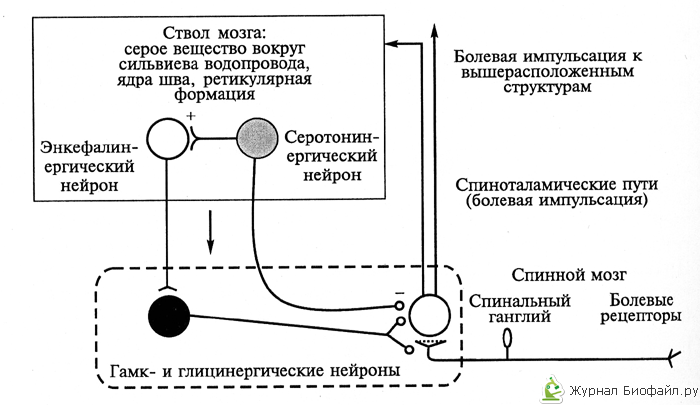
Рис.1.
Взаимодействие основных элементов
обезболивающей системы первого уровня:
ствол мозга – спиной мозг. (светлые
кружки – возбуждающие нейроны, черные
– тормозящие).
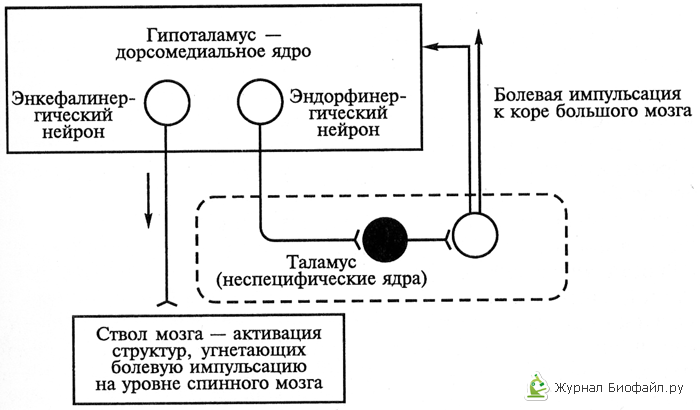
Рис.2.
Механизм работы обезболивающей системы
организма второго уровня (гипоталамус
– таламус – ствол мозга) с помощью
опиоидов.
Светлые
кружки – возбуждающие нейроны, черные
— тормозящие.
Степень
выраженности болевого ощущения не
определяется одной лишь силой экзогенного
или эндогенного болевого воздействия.
Во многом оно зависит от соотношения
активносте


